
Deze oefentoets bestaat uit zes vragen over het onderwerp evenwichten.
De uitwerking vind je na het openen van alle hints. Let op, als er geen ‘Controleer antwoord’ knop staat, moet je zelf je antwoord controleren met behulp van de hints en uitwerking.
Vraag 1
Deze vraag gaat over de volgende evenwichtsreactie:
2 SO2(g) + O2(g) 2 SO3(g)
In een ruimte van 1,0 liter wordt 10 mol zwaveldioxide samengebracht met 15 mol zuurstof. Na het instellen van het evenwicht is er nog 25% van het zwaveldioxide over.
Vraag 2
Gegeven is de volgende evenwichtsreactie: 2 C(s) + CO2(g) 2 CO(g).
Bij T=750 K geldt dat de waarde van K gelijk is aan 1,6*10–3. De concentratie van koolstofdioxide is na instellen van het evenwicht 1,5 M.
Vraag 3
Op een tijdstip t0 wordt in een vat 40 mol stikstof gemengd met een hoeveelheid waterstof. Op tijdstip t1 heeft zich het volgende evenwicht ingesteld:
N2(g) + 3 H2(g) 2 NH3(g).
De hoeveelheid waterstof is uitgezet tegen de tijd:
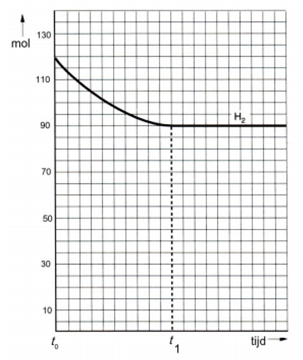
De lijn in de grafiek loopt na t1 horizontaal.
Bij kamertemperatuur ligt het evenwicht vrijwel geheel aan de kant van ammoniak. Bij hogere temperatuur is in het evenwichtsmengsel minder ammoniak aanwezig. Toch werkt men bij de ammoniakproductie met temperaturen boven de 400 ºC.
Vraag 4
Muskxyleen (MX) is een stof die gebruikt wordt bij de productie van parfums. Muskxyleen kan worden aangetoond in oppervlaktewater en in het vetweefsel van vissen en mensen. Omdat Muskxyleen mogelijk kankerverwekkend kan zijn is het gebruik sterk teruggedrongen.
Uit kwalitatief onderzoek aan vissen bleek dat MX wordt opgenomen uit het water via de huid, waarna het zich in het onderhuids vetweefsel ophoopt.
Onderzoekers stelden de hypothese op dat MX de huid in beide richtingen kan passeren. Het verdelingsevenwicht van MX in het water en in het vetweefsel kan worden voorgesteld als:
MX (aq) ⇄ MX (vet)
Op basis van modelproeven leidden de onderzoekers af dat de waarde van de evenwichtsconstante K van bovengenoemd evenwicht ongeveer 4·103 moest bedragen. Om deze waarde te toetsen, werd een kwantitatief onderzoek aan vissen uitgevoerd. In een aquarium werden vissen blootgesteld aan een constant gehalte MX van 22,5 nanogram MX per liter. Men stelde vast dat [MX (vet) ] in het vetweefsel van de vissen aanvankelijk snel steeg, maar zich na enige tijd stabiliseerde bij 105 microgram MX per liter vet.
Vraag 5
Het oplosbaarheidsproduct van magnesiumhydroxide is 5,6*10–12.
Een oplosbaarheid van magnesiumhydroxide veranderd als je het probeert op te lossen in een oplossing waarin al hydroxide ionen aanwezig zijn. Voor een bepaalde oplossing geldt [OH–] = 1,0·10–2 M.
Vraag 6
Stel het volgende homogene gasfase-evenwicht:
A + 2 B ⇄ C + D
De evenwichtsconstante van dit evenwicht is 8, de evenwichtsconcentratie van A is gelijk aan de concentratie B, beide zijn 2,00 M.














