Het hele PWS is te downloaden helemaal bovenaan de pagina.
Inhoudsopgave
Samenvatting
Fosfaat is een belangrijke verbinding op aarde en is nuttig voor allerlei toepassingen. Fosfaat wordt gewonnen uit mijnen, een vervuilend en niet-hernieuwbaar proces. Na huishoudelijk en agricultureel gebruikt te zijn, belandt fosfaat in hoge concentraties in afvalwater. Als dit water uiteindelijk wordt geloosd in oppervlaktewater, vindt er eutrofiëring plaats. Ook blijft op deze manier het ontginnen van fosfaat noodzakelijk. Om een stap te zetten richting een gesloten fosforcyclus is het daarom belangrijk dat fosfaat uit het afvalwater verwijderd wordt. Dit kan gedaan worden met fosfaatzouten. Twee van deze zouten zijn struviet en vivianiet. In dit onderzoek worden struviet en vivianiet met elkaar vergeleken op basis van a) fosfaatopbrengst bij verschillende temperaturen (0 °C, 20 °C, 30 °C) en b) duurzaamheid op het gebied van energieverbruik, economie en milieu-impact van de benodigde grondstoffen voor en het proces van Er is gebleken dat struviet een hogere fosfaatopbrengst heeft dan vivianiet en minder temperatuurafhankelijk is tijdens het neerslaan. Bij vivianiet is de duurzaamheid beter. Door onduidelijke resultaten bij de vivianietneerslag is het lastig een duidelijke conclusie te trekken. Vervolgonderzoek zal nodig zijn om de uiteindelijke betere methode van fosfaatverwijdering en -herwinning goed te bepalen.
Phosphate is an important chemical compound on earth which is useful for a variety of applications. Phosphate is mined – a polluting and non-renewable process. After being domestically or agriculturally used, phosphate ends up in wastewater in high concentrations, which in turn causes eutrophication when dumped in surface water. Additionally, mining phosphate remains necessary. Taking a step in closing the phosphorus cycle, phosphate can be removed from wastewater using phosphate salts that retrieve phosphate. Two examples are struvite and vivianite. In this study, struvite and vivianite are compared regarding a) yield at different temperatures (0 °C, 20 °C, 30 °C) and b) sustainability, considering energy use, economy and environmental toxicity. Struvite was found to have a higher yield than vivianite and appears to be more resilient to temperature changes during precipitation. Vivianite was found to be more sustainable though. Due to inconclusive results from the vivianite precipitation, a clear conclusion cannot be drawn from this study. Follow-up studies are recommended to determine the preferable phosphate salt on phosphate removal and recycling.
1. Inleiding
1.1 Fosfor en fosfaat
Fosfor (P), of zoals het nagenoeg exclusief in de natuur gevonden wordt, fosfaat (PO 3-), ligt aan de basis van leven. Fosfaat is nodig om DNA, RNA en celmembranen te vormen, maar ook voor het maken van botten en tanden (Foster et al., 2008). In verhouding tot andere belangrijke elementen die essentieel zijn voor leven, zoals stikstof (N) en kalium (K), is P in veel mindere mate aanwezig, waardoor het ook wel de bottleneck of life wordt genoemd (Isaac Asimov, 1974).
In de natuurlijke fosforcyclus komen fosforbevattende mineralen in de bodem en in water terecht (Ruttenberg, 2014) (figuur 1.1). Hier nemen microben en planten het fosfor op. Vervolgens eten dieren de planten op, waardoor ook zij fosfor in hun systeem krijgen. Door uitscheiding van dieren en decompositie van planten komt P weer terug in de aarde en is de cyclus rond. Fosfor vindt, buiten het menselijk en dierlijk lichaam, een belangrijke functie in agricultuur als mestbestanddeel en onder andere ook in vlamvertragers en schoonmaakproducten. Het fosfaat dat hiervoor nodig is, wordt verkregen door fosfaaterts te mijnen. Dit bestaat vooral uit apatiet (Ca5(PO4)3X, (X = OH, F, Cl)). Om fosfaat uit apatiet te verkrijgen zijn verschillende processen mogelijk. De eerste methode is het natte proces, waarmee 98 % van het fosfaaterts wordt behandeld om zo fosforzuur te winnen: zie reactievergelijking (1) (Gantner, Schipper, & Weigand, 2014). De tweede, maar weinig gebruikte methode om fosfaat te verkrijgen uit fosfaaterts is het thermale proces: zie reactievergelijking (2) (Environmental Protection Agency, 1980).
𝐶𝑎5(𝑃𝑂4)3𝐹 + 5 𝐻2𝑆𝑂4 + 5n 𝐻2𝑂 ⟶ 3 𝐻3𝑃𝑂4 + 5 𝐶𝑎𝑆𝑂4 ∙ n 𝐻2𝑂 + 𝐻𝐹 (n = 0; 0,5; of 2) (1)
4 𝐶𝑎5(𝑃𝑂4)3𝐹 + 18 𝑆𝑖𝑂2 + 30 C ⟶ 3 𝑃4 + 30 𝐶𝑂 + 18 𝐶𝑎𝑆𝑖𝑂3 + 2 𝐶𝑎𝐹2 (2)
Zowel het natte als het thermale proces hebben echter grote nadelen. Het natte proces produceert naast het fosforzuur (H3PO4) ook fosforgips (CaSO4 ⋅ n H2O). Per ton fosforzuur is dit ongeveer vijf ton fosforgips. Het grootste gedeelte van dit afvalproduct belandt op de vuilnisbelt (88 %) of wordt geloosd in zeewater (10 %) (Rychkov et al., 2018). Het thermale proces wordt voor 2 % van fosfaaterts toegepast en produceert niet zoveel afval, maar kost wel meer energie in verhouding tot het natte proces, 12,5 – 14 MWh per ton P4 (Gantner et al., 2014). Dit komt doordat het thermale proces een temperatuur van 1500-1600 °C vereist, in tegenstelling tot het natte proces, dat functioneert bij een temperatuur van 70-80 °C.
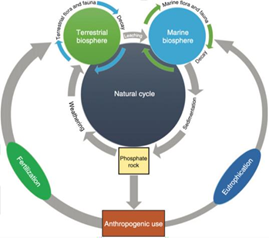
Figuur 1.1. Schematische representatie van de natuurlijke fosforcyclus en de invloed van menselijk gebruik. Uit: Beijer & Slootweg (2021).
1.2 Fosfaatafval
Veel van het fosfaat dat uit deze reacties vrijkomt, komt uiteindelijk, na gebruik in bovengenoemde toepassingen, weer in afvalstromen terecht. Dit zorgt ervoor dat fosfaat steeds uit mijnen gewonnen moet worden om te kunnen voldoen aan de blijvende vraag naar fosfaat. Omdat fosfaat niet herwonnen wordt uit afvalstromen, is de fosforcyclus niet gesloten en is er steeds nieuw fosfaat nodig uit fosfaaterts. Dit is geen duurzaam proces (Beijer & Slootweg, 2021). Het draagt dan ook niet bij aan de duurzamere wereld die de VN met haar Duurzame Ontwikkelingsdoelen (SDG’s) wil realiseren (UN-DESA, 2015). Om de fosforcyclus te sluiten is het dus belangrijk om fosfaat te herwinnen uit afvalstromen. Op die manier hoeft er geen fosfaaterts meer ontgonnen te worden.
Eén van de grootste afvalstromen is huishoudelijk afvalwater (Van Dijk, Lesschen, & Oenema, 2016). Dit afvalwater komt bij afvalwaterzuiveringsinstallaties terecht (AWZI’s). In AWZI’s wordt afvalwater gezuiverd om het zo schoon mogelijk te kunnen lozen in oppervlaktewater. Wanneer dit niet gebeurt, kan eutrofiëring, een proces dat biodiversiteit verminderd door een overmaat aan nutriënten zoals N, worden voorkomen (Stuart Chapin, Matson, & Vitousek, 2012). Eutrofiëring kan echter ook komen door een overmaat aan P in vorm van fosfaat (Environmental Protection Agency, 2021). Bij de zuivering wordt fosfaat dus ook gezuiverd uit het afvalwater, waar het in verschillende vormen voorkomt. Het afvalwater uit de veesector bevat vaak veel organische fosfaten (Wang, Gao, Fan, & Jin, 2011), terwijl in huishoudelijk afvalwater anorganisch fosfaat het meest voorkomt. Er zijn twee manieren waarop fosfaat uit afvalwater wordt verwijderd: verbeterde biologische fosforverwijdering (VBFV) en chemische precipitatie van metaalfosfaten.
1.3 Fosfaatverwijdering
De eerste manier, VBFV, haalt op een biologische manier fosfaat uit afvalwater. Afwisselende aerobe en anaerobe omstandigheden zorgen ervoor dat microben, bekend als polyfosfaat-verzamelende organismen, P kunnen opnemen uit het afvalwater. Op deze manier kan P uit het water naar het slib verplaatst worden, waar de concentratie P twee tot vijf keer hoger kan zijn dan vóór VBFV (Liao, Wong, & Lo, 2005).
De tweede manier is een vrij eenvoudig proces dat gebaseerd is op het toevoegen van ijzer-, aluminium- of ander metaalzouten in de vorm van chlorides of sulfaten, die samen met het fosfaat als onoplosbare fosfaatzouten neerslaan. Deze kunnen vervolgens verwijderd worden uit het afvalwater (Morse, Brett, Guy, & Lester, 1998). Struviet, reactievergelijking (3), en vivianiet, reactievergelijking (4), zijn twee van deze fosfaatzouten die worden gebruikt voor het verwijderen van fosfaat uit afvalwater (Wu et al., 2019; Z. Ye et al., 2014).
𝑀𝑔2+ + 𝑁𝐻4+ + 𝑃𝑂43− + 6 𝐻2𝑂 → 𝑀𝑔(𝑁𝐻4)𝑃𝑂4 ∙ 6 𝐻2𝑂 (3)
3 𝐹𝑒2+ + 2 𝑃𝑂43− + 8 𝐻2𝑂 → 𝐹𝑒3(𝑃𝑂4)2 ∙ 8 𝐻2𝑂 (4)
Het verwijderen van het fosfaat door struviet en vivianiet neer te laten slaan zorgt op zich nog niet voor een gesloten fosforcyclus. Daarvoor moet het fosfaat nog uit het struviet en vivianiet herwonnen worden. Dit is een onderzoeksveld waar SusPhos (NWO, 2021) en Wetsus (2021) onderzoek in doen.
Zowel het winnen van struviet als het winnen van struviet zijn duurzame methodes om fosfaat uit het afvalwater te verwijderen. Dit is goed te zien wanneer de methodes met de door de VN opgestelde SDG’s worden vergeleken (figuur 1.2) (UN-DESA, 2015). Zo draagt fosfaatverwijdering uit afvalwater allereerst bij aan het veertiende doel (leven in het water). Door het zuiveren blijft het oppervlaktewater idealiter schoon bij lozing. Zo wordt er, door eutrofiëring te voorkomen, ook aan doel vijftien (leven op het land) bijgedragen. Er zijn echter ook andere SDG’s waar deze methodes aan bijdragen. Door de herwonnen stoffen opnieuw te gebruiken in de industrie draagt de verwijdering van fosfaat ook bij aan het elfde SDG (duurzame steden en gemeenschappen). Tenslotte wordt ook aan het twaalfde punt op de agenda van de VN bijgedragen. Verantwoorde consumptie en productie wordt namelijk gerealiseerd door het hergebruik van afvalstoffen. Het doel van de fosfaatverwijdering, namelijk het sluiten van de fosforcyclus, laat ook SDG 12 zien.


Figuur 1.2. De door de VN opgestelde Duurzame Ontwikkelingsdoelen (UN-DESA, 2022).
1.4 Onderzoeksvragen
In dit onderzoek wordt gekeken naar de tweede manier om fosfaat te verwijderen uit afvalwater: de chemische precipitatie van metaalfosfaten. Dit is een methode die al veel wordt toegepast in AWZI’s. Aluminium- en ijzer (III)fosfaat zijn hierbij de meest toegepaste fosfaatzouten om P uit het afvalwater te verwijderen. Met het oog op veiligheid, fosfaatwinning en hergebruik zijn struviet (Mg(NH4)PO4) en vivianiet (Fe3(PO4)2) echter betere opties (Fodoué, Nguetnkam, Tchameni, Basga, & Penaye, 2015; Santa Cruz Biotechnology, 2010; Szymańska et al., 2019; Talboys et al., 2016; ViviMag, 2022). In het verleden is al veel onderzoek gedaan naar de omstandigheden waaronder deze zouten het beste vormen. Beginstoffen, de concentraties daarvan en pH zijn daarbij belangrijke factoren.
Zo is er bijvoorbeeld onderzocht of er meer struviet ontstaat bij het toevoegen van magnesiumchloride of bij het toevoegen van magnesiumsulfide (Desmidt et al., 2015; Jupp, Beijer, Narain, Schipper, & Slootweg, 2021). Temperatuur kan echter ook van grote invloed zijn op de oplosbaarheid van zouten. Temperatuur is sterk wisselend in real-life situaties. Zo kunnen er bij AWZI’s watertemperaturen van ongeveer 0 °C tot 30 °C voorkomen. Naast de efficiëntie van de neerslag (dat is de relatieve terugwinning, het percentage van het in origineel afvalwater aanwezige fosfaat dat herwonnen is) is ook de duurzaamheid van belang, zodat efficiëntere fosfaatverwijdering niet ten koste gaat van duurzaamheid. Deze aspecten worden in dit onderzoek bekeken en met elkaar verbonden. Hiervoor is de volgende vraag opgesteld:
Is het verwijderen van fosfaat bij 0 °C, 20 °C en 30 °C uit synthetisch afvalwater gedurende twee uur duurzamer op het gebied van effiëntie en op het gebied van energie, economie en milieu-impact van de benodigde grondstoffen voor en het proces van fosfaatherwinning door vorming van struviet of door vorming van vivianiet?
Om een antwoord te kunnen geven op deze vraag, zijn er enkele deelvragen geformuleerd. Allereerst is het belangrijk om te weten wat de daadwerkelijke efficiëntie is van de fosfaatverwijdering bij verschillende temperaturen. Om dat te onderzoeken is de volgende, praktische deelvraag opgesteld.
- Is de efficiëntie van fosfaatverwijdering uit synthetisch afvalwater na twee uur bij 0 °C, 20 °C en 30 °C hoger door vorming van struviet of door vorming van vivianiet?
Volgens Desmidt et al. (2015) kan met een equimolaire hoeveelheid P en Mg bij een pH van 8-9 90 % van P worden verwijderd uit afvalwater. Deze verhouding is echter niet optimaal. Een stoichiometrische verhouding (theoretische molverhouding) waarbij magnesium relatief meer aanwezig is, zorgt voor meer neerslag, zoals blijkt uit onderzoek van Liu et al. (2018). Uit dat onderzoek blijkt echter ook dat pH meer invloed heeft dan de verhouding tussen magnesium en fosfaat. Bij een pH van 9 is de verwachting dan ook een maximale efficiëntie van 90 % bij kamertemperatuur (20 °C). Bij een temperatuur van 0 °C zijn zouten slechter oplosbaar. Bij deze temperatuur zal dus waarschijnlijk een minimale efficiëntie van 90 % gelden. De temperatuur van 30 °C heeft waarschijnlijk een negatief effect op de efficiëntie, aangezien de oplosbaarheid van zouten groter wordt bij hogere temperaturen. Dit zou resulteren in minder neerslag en dus een lagere efficiëntie.
Bij de neerslag van vivianiet is de concentratie Fe2+ van groot belang en kan de efficiëntie van fosfaatverwijdering oplopen tot 70-90 % bij een verhouding Fe:P van 1:2,5 (Wilfert et al., 2018). Over de verhouding van 1,5 die in dit onderzoek gebruikt wordt (zie materiaal en methode), schrijft Wilfert en ook Cao (2019) dat er 60-85 % gebonden wordt. Vivianiet slaat minder goed neer bij hogere temperaturen, in dit geval boven de 32 °C, net als de meeste zouten (Prot, Korving, Dugulan, Goubitz, & Van Loosdrecht, 2021). Verwacht wordt dat dit effect ook al te merken zal zijn bij 30 °C. Struviet met vivianiet vergelijkend wordt verwacht dat struviet een hogere efficiëntie zal hebben bij 20 °C, aangezien de fosfaatzouten respectievelijk efficiënties van 90 % en 85 % hebben in de literatuur. Verwacht wordt dat de trend dat struviet een hogere efficiëntie heeft zich voortzet bij 0 °C en 30 °C.
Het neerslaan van de fosfaatzouten in dit onderzoek is beperkt tot een tijdsduur van twee uur, omdat dan zeker is dat de reactie verlopen is. Sommige studies spreken over een reactieduur van 15-20 minuten (Siciliano, Limonti, Curcio, & Molinari, 2020), andere over minuten (Kabdaşlı, Parsons, & Tunay, 2006). In ieder geval kan met grote waarschijnlijkheid gezegd worden dat de neerslagreactie na twee uur voltooid is.
1.4.1 Duurzaamheid struviet en vivianiet
Ook is onderzoek nodig naar de duurzaamheid van de methodes die gebruikt worden om struviet en vivianiet neer te laten slaan. Het herwinnen van fosfaat uit struviet en vivianiet is ook belangrijk om hierin mee te nemen, aangezien het belangrijk is dat deze methodes niet minder duurzaam zijn dan het alternatief. Dat is namelijk het verkrijgen van fosfaat uit fosfaaterts door middel van het natte of thermale proces. Zoals eerder beschreven zijn energieverbruik, economie en milieu- impact belangrijke aspecten bij het bepalen van de duurzaamheid van het natte of thermale proces. Deze aspecten worden daarom ook bij de gebruikte fosfaatzouten in dit onderzoek bekeken. Daarvoor is de volgende theoretische deelvraag opgesteld.
- Is de vorming van struviet of de vorming van vivianiet uit synthetisch afvalwater duurzamer op het gebied van economie, energie en milieu-impact van de benodigde grondstoffen voor en het proces van fosfaatherwinning?
2. Praktische deelvraag
2.1 Methode
Zie voor een uitgebreide beschrijving van de methode en de materiaallijst respectievelijk bijlage A en B.
Struviet en vivianiet zijn in dit onderzoek bij drie verschillende temperaturen gevormd: in een ijsbad (0 °C), op kamertemperatuur (20 °C) en in een verwarmd zandbad (30 °C). Door monoammoniumfosfaat, ammoniumchloride, magnesiumchloride en ijzer(II)chloride in de juiste concentraties toe te voegen ontstonden struviet en vivianiet, die na twee uur werden gefilterd en gewogen. Voor de vorming van struviet is een pH van 9 nodig en voor de vorming van vivianiet een pH van 7. Ook moet vivianiet onder zuurstofarme omstandigheden gevormd worden in verband met het oxideren van ijzerionen.
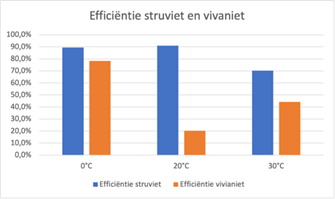
Figuur 2.1. De efficiëntie van struviet en vivianiet bij 0 °C, 20 °C en 30 °C.
2.2 Resultaten
De efficiëntie van struviet en vivianiet bij verschillende temperaturen is weergegeven in figuur 2.1. Bij een temperatuur van 0 °C heeft struviet een efficiëntie van 89,5 % en vivianiet een efficiëntie van 78,4 %. Bij een temperatuur van 20 °C realiseert struviet een efficiëntie van 91,0 % en vivianiet een van 20,2 %. Bij 30 °C heeft struviet een efficiëntie van 70,2 % en vivianiet van 44,3 %.
2.2.1 Struviet bij verschillende temperaturen
De efficiëntie van struviet is het hoogst bij een temperatuur van 20 °C. Hierbij is nauwelijks verschil met de efficiëntie bij 20 °C. Wel is er verschil tussen de efficiëntie bij 0 °C en 20 °C met die bij 30 °C. De efficiëntie bij 30 °C is namelijk lager.
2.2.2 Vivianiet bij verschillende temperaturen
Struviet heeft de hoogste efficiëntie bij een temperatuur van 0°C en de laagste bij een temperatuur van 30 °C. De efficiëntie van vivianiet bij 20 °C wijkt af ten opzichte van de vivianietefficiëntie bij 0 °C en 30 °C als rekening wordt gehouden met hoe struviet zich gedraagt bij de verschillende temperaturen.
2.2.3 Struviet en vivianiet vergeleken
Bij alle temperaturen heeft struviet een hogere efficiëntie dan vivianiet. Hierbij is het verschil tussen struviet en vivianiet bij een temperatuur van 20 °C het grootst. Daarnaast bevat deze temperatuur bij struviet de hoogste en bij vivianiet de laagste waarde van de betreffende fosfaatzouten. Waar struviet bij een temperatuur van 20 °C de hoogste efficiëntie heeft, heeft vivianiet bij deze temperatuur de laagste. De verschillen tussen de drie temperaturen zijn bij struviet het kleinst.
2.3.4 Waarnemingen
Tijdens de reactie
Gedurende de twee uur zijn alle oplossingen voor de vorming van struviet na toevoeging van magnesium troebel geworden. Van helder kleurloos gingen alle oplossingen naar troebel wit. Gedurende deze tijd waren de vivianietoplossingen ook troebel en veranderde de kleur naar blauw.
Filtratie
Bij struviet bestond het residu uit kleine, losse, witte schilfers (afbeelding 2.1). Na filtratie was het filtraat bij alle temperaturen helder. Bij vivianiet was het residu niet los te onderscheiden van het filter en was het residu na de filtratie blauwgekleurd (afbeelding 2.2). Bij de filtratie van vivianiet bij 0 °C en 30 °C scheurde het filter. Dit filter is gedroogd en gewogen met het deel van de opbrengst wat op dit filter aanwezig was. Bij beide oplossingen is het filtraat teruggegoten in de schlenk en zijn de oplossingen met een nieuw filter gefiltreerd. Hierna waren de oplossingen nog steeds blauw. Na nog een filtratie met ditzelfde filter waren beide oplossingen kleurloos. Vervolgens is ook dit filter gedroogd en gewogen. Bij 20 °C vivianiet scheurde het filter niet en was de vloeistof na de eerste filtratie kleurloos en is het filter na deze eerste filtratie gedroogd en gewogen.
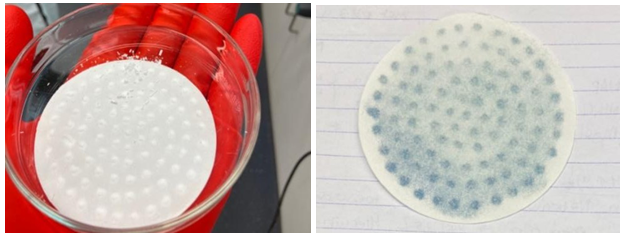
Afbeelding 2.1. Filter en residu struvietfiltratie. Afbeelding 2.2. Filter en residu vivianietfiltratie
2.3 Discussie experimentele resultaten
Uit de resultaten blijkt als eerste dat de efficiëntie van struviet bij alle temperaturen groter is dan die van vivianiet. Dit klopt met de hypothese over de efficiëntie, aangezien het rendement van struviet hoger is dan dat van vivianiet. In dit onderzoek is gekeken naar één concentratie voor beide struviet en vivianiet. Het zou kunnen dat vivianiet bij andere concentraties een beter rendement heeft, waarbij de efficiëntie van vivianiet wellicht die van struviet kan overschrijden. Andere mogelijke oorzaken kunnen oxidatie of niet goed werkende filters zijn. Zie hiervoor het kopje ‘Afwijking vivianiet’.
De efficiëntie van de fosfaatverwijdering door struviet komt overeen met de hypothese over de temperatuur. De efficiëntie bij 0 °C en 20 °C is namelijk ongeveer 90 % en de efficiëntie bij 30°C is lager. Dit laatste komt echter niet overeen met ongepubliceerd onderzoek van S. Beijer, waarin vermeld wordt dat een temperatuur van 50 °C weinig invloed heeft op de mate van neerslag. Vervolgonderzoek kan nuttig zijn, zie hiervoor het kopje ‘Vervolgonderzoek’.
In tegenstelling tot struviet, komt de efficiëntie van vivianiet niet overeen met de hypothese over de temperatuur. De verwachting was dat de efficiëntie bij 0 °C en 20 °C tussen de 70 % en 90 % zou vallen. Bij 0 °C is dit inderdaad het geval, maar bij 20 °C niet. Daar is de efficiëntie maar 20,2 %, wat buiten de verwachting ligt als het met de struvietefficiënties wordt vergeleken. Ook zou er bij 30 °C minder neerslag ontstaan dan bij 20 °C, wat niet het geval is. In plaats van minder neerslag is er juist meer gevormd. Dit is de tweede reden waarom de neerslag van 20 °C waarschijnlijk afwijkt. Vanwege deze afwijking is de hypothese echter wél te bevestigen wanneer de efficiënties van 0 °C en 30°C worden vergeleken: de efficiëntie is dan bij een hogere temperatuur veel lager.
2.3.1 Afwijking vivianiet
Extra filtratie
De afwijking bij 20 °C van vivianiet kan verschillende redenen hebben. Ten eerste is het synthetische afvalwater bij de filtratie van 20 °C maar met één filter gefiltreerd, in tegenstelling tot 0 °C en 30 °C, die met twee filters gefiltreerd zijn. Dit kwam doordat de filters scheurden bij de Büchner-filtratie, wat bij geen van de struvietfiltraties gebeurde en ook niet bij 20 °C vivianiet. Het scheuren van de filters kan komen door een verschil in deeltjesgrootte bij het vivianiet, waarbij het niet scheuren bij 20°C puur toeval is (Korving, 2018). Er is echter geen ondersteunende literatuur die bevestigt dat filters door vivianiet scheuren. Een andere mogelijkheid is dat het gebruikte filterpapier van lage kwaliteit is en daardoor makkelijk scheurt. Ook over deze mogelijkheid is verder geen ondersteunende literatuur te vinden. Om dit verder te onderzoeken kan vervolgonderzoek nuttig zijn, zie ‘Vervolgonderzoek’.
Helderheid filtraat
Het filtraat bij 0 °C en 30 °C is na de filtratie door deze twee filters nog blauw, wat kan wijzen op achtergebleven neerslag. Deze filtraten zijn vervolgens nog een keer gefilterd, waarna ze kleurloos waren. Dit is niet met het filtraat van 20 °C gedaan, omdat dat filtraat helder was. Bij het filteren is wellicht een te snelle conclusie getrokken dat de kleurloze oplossing erop wees dat alle neerslag gefilterd was. Het zou namelijk ook kunnen dat de oplossing er kleurloos uitzag, terwijl er nog wel vivianietdeeltjes aanwezig waren. Omdat struvietdeeltjes groter zijn dan vivianietdeeltjes zou dat de afwijking bij vivianiet, die niet bij struviet voorkomt, kunnen verklaren (Korving, 2018). Als dus niet alle neerslag is gefiltreerd, wijst het verschil in gewicht erop dat er bij een tweede filtratie nog veel vivianiet kan neerslaan. Op grote schaal wordt vivianiet echter verwijderd uit het afvalwater met behulp van magneten, waardoor het scheuren van filterpapier daar geen problemen vormt (Prot et al., 2019).
Oxidatie
Bij alle experimenten van vivianiet kan de efficiëntie mogelijk iets afwijken door onbedoelde oxidatie. Omdat het synthetische afvalwater met neerslag niet compleet zuurstofarm kan worden gefiltreerd, is het mogelijk dat onder invloed van zuurstof, een aantal Fe2+-ionen zijn geoxideerd naar Fe3+. Daardoor zouden in plaats van vivianiet (Fe3(PO4)2) andere fosfaatzouten kunnen ontstaan (bijvoorbeeld Fe2+2Fe3+(PO4)2(OH)·(H2O)7) die andere molaire massa’s hebben. De blauwe kleur van de oplossingen zoals beschreven bij ‘Resultaten – Waarnemingen’ wijst hierop. Door onbedoelde oxidatie zou de efficiëntie hoger kunnen zijn dan de nu berekende waardes. Dat het gevormde vivianiet oxideert, blijkt uit de blauwe kleur, wat wijst op oxidatie volgens McCammons en Burns (1980) en Wu (2019).
2.3.2 Reactietijd
De gebruikte reactietijd is mogelijk wat te lang. In tegenstelling tot Siciliano (2020) en Kabdaşlı (2006), beschrijft Buchynska (2017) dat de oplossingen na 20 minuten meer neerslag hebben dan na 60 minuten. Dit kan ook invloed hebben op de uiteindelijke efficiëntie.
2.3.3 Temperatuur
Wat betreft de invloed van verschillende temperaturen op de neerslag van struviet en vivianiet: er zijn verschillen op te merken aan efficiënties bij de verschillende temperaturen. Zoals eerder vermeld is de efficiëntie bij hogere temperaturen bij zowel struviet als vivianiet lager. Dit kan gesteld worden ondanks het afwijkende resultaat van vivianiet bij 20 °C, want het verschil tussen 0 °C en 30 °C laat wel een betere efficiëntie bij lagere temperaturen zien. Hierin is de hypothese dus bevestigd. Dit houdt concreet in dat fosfaatverwijdering door struviet en vivianiet uit afvalwater op grotere schaal beter in de herfst/winter/lente zou werken dan in de zomer. Zeker in landen waar warme zomers (gemiddelde temp rond de 30 °C) voorkomen. Daarnaast lijkt struviet minder temperatuurafhankelijk te zijn, waardoor dit een betere optie is voor fosfaatverwijdering gedurende het hele jaar.
2.3.4 Fosfaatneerslag, efficiëntie
Bij alle temperaturen is de relatieve efficiëntie bij struviet hoger dan bij vivianiet. Dit betekent dat het verwijderen van fosfaat door vorming van struviet efficiënter is dan door vorming van vivianiet. Het kan echter wel zo zijn dat de resultaten van vivianiet afwijken van de werkelijke neerslagmassa’s. Ook zou het kunnen dat de verhoudingen tussen struviet en vivianiet bij andere concentraties anders liggen. Aan de hand van dit onderzoek kan echter gesteld worden dat qua efficiëntie struviet de betere keuze is.
3. Theoretische deelvraag
Struviet en vivianiet worden beoordeeld op duurzaamheid aan de hand van de 12 uitgangspunten voor Groene Chemie (zie figuur 3.1) zoals die zijn opgesteld door de Environmental Protection Agency (EPA) (1998). Hierbij wordt gekeken naar de aspecten energie, economie en milieu.

Figuur 3.1. De 12 groene chemie uitgangspunten opgesteld door de Environmental Protection Agency (1998).
3.1 Duurzaamheid struviet
3.1.1 Energie en economie
Toevoegen van magnesium
In reactievergelijking (3) is te zien dat er voor het vormen van struviet magnesium, ammonium, fosfaat en water nodig is. In afvalwater zijn ammonium en fosfaat aanwezig (Henze, Harremoes, Arvin, & la Cour Jansen, 2001). Magnesium is niet voldoende aanwezig. Daarom wordt er MgCl2 aan het afvalwater toegevoegd.
MgCl2, MgSO4 en MgO zijn de meest gebruikte bronnen voor het toevoegen van magnesium aan afvalwater. Deze grondstoffen worden bij verschillende technologieën zoals Phosnix, Pearl Ostara en Phospaq commercieel gebruikt voor het winnen van struviet (Kataki, West, Clarke, & Baruah, 2016). Een nadeel is dat het toevoegen van magnesium zorgt voor hoge productiekosten, namelijk 75 % van de totale kosten van struvietwinning (Ashley, Mavinic, & Koch, 2009). Verder moet het afvalwater geroerd worden om struviet goed te laten neerslaan. Hiervoor is mengenergie nodig (Muryanto, 2017). De energiekosten zullen hierdoor dus stijgen. Bij vorming van struviet wordt uitgangspunt 6 (Energie-efficiënt ontwerpen), dat ook betrekking heeft op kosten, dus op deze fronten niet behaald. Struviet verbruikt echter wel minder energie dan het thermale proces (Gantner et al., 2014; Ghangrekar, Sathe, & Das, 2021).
pH-waarde
De vorming van struviet is optimaal bij een pH van 9 (Desmidt et al., 2015). Aangezien de pH van afvalwater rond de 7 ligt, wordt de pH verhoogd door het toevoegen van NaOH. Door middel van NaOH als katalysator bijvoorbeeld wel aan uitgangspunt 9 (Katalyse) voldaan.
3.1.2 Milieu
Schade van productiemethode
De milieu-impact van de productieprocessen van NaOH is per kilo ongeveer 0,86 kg CO2 (Hofman & van den Brand, 2020). Deze uitstoot moet vermeden worden met het oog op uitgangspunt 3 (Minder schadelijke chemische productiemethoden) (Solomon, Plattner, Knutti, & Friedlingstein, 2009). NaOH kan echter weer uit afvalwater worden gehaald op verschillende manieren (Imran, Khan, Qazi, & Arshad, 2015; US Department of Energy, 1999). Er is dan een gesloten NaOH-cyclus, waarmee het nadeel van de CO2-uitstoot vervalt. Magnesium moet echter nog wel vervoerd worden, wat een bijdrage levert aan de CO2-uitstoot. Aan de andere kant heeft fosfaatwinning uit struviet weinig milieuimpact in vergelijking met het fosfaaterts dat uit mijnen gewonnen wordt. Zo produceert het, in tegenstelling tot het natte proces, geen bijproducten, zie reactievergelijking (1) en (3). In dit opzicht is dus juist aan uitgangspunt 3 voldaan.
Afvalverwijdering
In aansluiting hierop kan gezegd worden dat bij struvietvorming aan uitgangspunt 1 (Preventie), dat zich focust op het voorrkomen van afvalvorming, voldaan is. Door verwijdering van struviet uit afvalwater worden concentraties van de nutriënten N en P in afval-/lozingswater namelijk lager. Hierdoor heeft oppervlaktewater geen biodiversiteitsverlies door eutrofiëring te lijden. Op deze manier helpt struvietneerslag juist mee aan afvalverwijdering in plaats van dat het afval vormt. Als er namelijk te veel ammonium en fosfaat aanwezig is in water kan dit niet alleen tot eutrofiëring leiden (Environmental Protection Agency, 2021; Stuart Chapin et al., 2012), maar het kan ook giftig zijn voor bentische (de onderste laag van het water) of oppervlaktewater biota (Lapota, Duckworth, & Word, 2000) wanneer er te veel van achterblijft in het afvalwater of slib daarvan.
Hergebruik van magnesium
Stoffen die uit afvalwater gebonden worden, kunnen daarnaast via struviet hergebruikt worden. Struviet vindt als heel fosfaatzout momenteel een toepassing in kunstmest (Szymańska et al., 2019; Talboys et al., 2016), maar de losse stoffen in struviet kunnen ook een toepassing vinden. Aan uitgangspunt 7 (Gebruik van hernieuwbare grondstoffen) wordt deels voldaan bij struviet. De stoffen die in struviet zitten, namelijk fosfaat, ammonium en magnesium, kunnen uit struviet gehaald worden voor apart hergebruik, waarnaar SusPhos onderzoek doet (NWO, 2021). Zo wordt fosfaat uit struviet gehaald en wordt onderzoek gedaan naar toepassingen voor dit fosfaat. Ook het magnesiumzout dat bij fosfaatwinning ontstaat, wordt weer teruggeleid naar de AWZI voor nieuwe neerslag (VNCI, 2021). Wanneer dit hergebruik in de toekomst op grotere schaal geïntroduceerd wordt, is uitgangspunt 7 behaald en vervallen de nadelen van punt 6 met betrekking tot de hoge kosten voor magnesiumproductie ook.
Aan uitgangspunt 10 (Ontwerpen met het oog op afbraak) is deels voldaan. Uiteraard is struviet op zichzelf al wel afbreekbaar als bijvoorbeeld kunstmest. Bij SusPhos wordt echter ook gekeken naar verwijdering van fosfaat uit struviet én de vervolgstap hiervan, het vormen van bioafbreekbare stoffen voor toepassingen als brandwerende kleding. Daarom zal fosfaat in de toekomst waarschijnlijk ook aan dit punt voldoen, wat het belang van struviet in het kader van duurzaamheid vergroot.
Daarnaast wordt aan uitgangspunt 4 (Ontwikkelen van minder schadelijke chemische stoffen) voldaan, aangezien de bestandsdelen van struviet (Mg en N) juist plantengroei bevorderen in plaats van dat zij chemisch schadelijk zijn (Dhakal, 2008). Dit draagt bij aan het verduurzamen van onze aarde. Wel moet hierbij ook gelet worden op het voorkomen van eutrofiëring door het toevoegen van te veel nutriënten.
Medicijnresten
Voor uitgangspunt 4 geldt echter wel dat er geen medicijnresten in struviet moeten zitten. Een vervuilend aspect in struviet kunnen namelijk medicijnresten of pathogenen zijn. Dit komt door vervuiling van het afvalwater. Studies van Ye et al. (2017) en Kemacheevakul, Otani, Matsuda en Shimizu (2012) tonen aan dat medicijnresten zoals tetracycline kunnen absorberen aan het struvietkristal. Uit de studie van Morgenschweis, Vergouwen, Schöll en Leenen (2015) blijkt daarnaast dat metoprolol voorkomt in struviet. Volgens een briefrapport van het RIVM (van der Grinten & Spijker, 2017) geven de aangetroffen concentraties medicijnresten in struviet geen aanwijzingen voor concrete risico’s. Deze conclusie is echter zwak, omdat het op één monster gebaseerd is. Als er echter structureel medicijnresten voorkomen in het struviet, dan moet onderzocht worden of dit bij toepassing risico’s kan vormen voor het milieu. Theoretisch kan ophoping van medicijnresten in het milieu of opname ervan in voedselgewassen namelijk zorgen voor gezondheidsrisico’s. De binding van medicijnen aan struviet zou dan ook niet voldoen aan het vierde uitgangspunt. Het is dus nog onzeker of struviet op dit gebied schade aan het milieu veroorzaakt.
Chloor
Met het toevoegen van MgCl2 wordt er ook chloor aan het afvalwater toegevoegd. Chloor heeft een groot verspreidingspotentiaal en is een watergevaarlijke stof. Als chloor in te grote concentraties in afvalwater aanwezig is, kan het schade veroorzaken aan het milieu, dieren of mensen. Daarnaast kunnen chloorverbindingen ook toxisch en sterk milieugevaarlijk zijn. Aangezien de toegevoegde hoeveelheid chloor bij struviet niet groot is, veroorzaakt chloor bij struvietvorming geen milieuproblemen (Lenntech, 2022).
3.2 Duurzaamheid vivianiet
Toevoegen van ijzer
In de reactievergelijking (4) is te zien dat er voor het vormen van vivianiet Fe2+, fosfaat en water nodig is. Fosfaat is in afvalwater aanwezig (Henze et al., 2001). Om de neerslag van vivianiet zo stabiel mogelijk te laten verlopen is o.a. een grote hoeveelheid Fe2+, een hoge fosfaatactiviteit en een lage sulfideactiviteit nodig (Kwon et al., 2014). Wanneer vivianiet gevormd wordt met een Fe:P molverhouding van 3:1 wordt P bijna volledig verwijderd (Nriagu, 1972).
Bij de bereiding van drinkwater voor menselijke consumptie wordt ijzer uit grondwater gehaald (Koopmans, Chardon, Belder, & Groenenberg, 2011). Huishoudelijk afvalwater bevat dus lage concentraties ijzer. Volgens de Nederlandse Waterleidingbesluiten is de maximaal toegestane concentratie van ijzer in drinkwater 200 µg/L (Versteegh, Morgenstern, & Te Biesebeek, 2004). Uiteindelijk belandt dit water in afvalwater, waardoor dit afvalwater een te lage concentratie heeft voor de vorming van vivianiet. Op grote schaal moet daarom FeCl3 toegevoegd worden aan het afvalwater, dat in Fe2+ vorm reageert. Op grote schaal zorgen microben namelijk voor de omzetting van Fe3+ naar Fe2+ in het afvalwater (Rothe, Kleeberg, & Hupfer, 2016).
In dit onderzoek zijn microben echter afwezig ter bevordering van de controle over de omstandigheden. Dit betekent dat het nodig is dat het synthetisch afvalwater zuurstofarm is, waardoor het Fe2+ uit het toegevoegde FeCl2 niet kan oxideren naar Fe3+. Voor de vorming van vivianiet is een neutrale pH optimaal (Jupp et al., 2021), maar de pH in het zuurstofarme water is omstreeks 5-6. Om een neutrale pH in dit onderzoek te bereiken wordt NaOH toegevoegd. Op grote schaal heeft afvalwater echter wel een pH van ongeveer 7 – daarin worden uiteraard wel microben gebruikt – en is er dus geen NaOH nodig bij de vorming van vivianiet. Het toevoegen van NaOH speelt dus geen rol in eventuele duurzaamheids-overwegingen bij het gebruik van vivianiet.
3.2.1 Energie en economie
Energieverbruik
Voor de neerslagreactie van vivianiet wordt bij AZWI’s dus alleen Fe3+ toegevoegd aan afvalwater. Bij de productie van ijzer reageert koolstof onder hoge temperaturen met de zuurstof uit ijzererts. De productie van ijzer uit erts kost veel energie, 19.8–31.2 GJ per ton (Yang, Raipala, & Holappa, 2014). Als het gaat om uitgangspunt 6 (Energie-efficient ontwerpen) is ijzerproductie dus niet duurzaam.
De neerslagreactie van vivianiet zelf lijkt echter energieneutraal of zelfs energiewinnend te zijn (Prot et al., 2021). Er is echter wel mengenergie nodig om vivianiet optimaal neer te laten slaan (Zhang, 2012). Nadat vivianiet gevormd is, is het lastig uit het afvalwater te halen in verband met een kleine deeltjesgrootte (Korving, 2018). Het paramagnetische (zelf niet magnetisch, maar wel magnetisch in de buurt van een grote magneet) karakter van vivianiet zou echter een goede basis voor een scheidingstechniek kunnen creëren: een onderwerp waar Wetsus onder het project ViviMag onderzoek naar doet (Wetsus, 2021). Er is echter wel langdurig veel energie nodig om een sterk magnetisch veld te onderhouden (Frederichs, von Dobeneck, Bleil, & Dekkers, 2003). Uit deze zaken blijkt dus dat het proces van vivianiet qua neerslag met uitgangspunt 6 overeenstemd, maar qua scheiding uit afvalwater in AZWI’s niet.
Oorspronkelijke omstandigheden
Bij het vormen van vivianiet zijn, behalve het toevoegen van Fe3+ en het behouden van een magnetisch veld, geen aanpassingen van de omstandigheden vereist zoals die in afvalwater al zijn. De vorming vindt bijvoorbeeld plaats bij een pH van 7 en ook de aanwezigheid van sulfide heeft geen invloed op de vorming van vivianiet (Azam et al., 2019). Daarnaast zijn geen katalysatoren nodig. Op dit gebied voldoet vivianietneerslag dus aan punt 9 (Katalyse).
3.2.2 Milieu
Hergebruik van ijzer
Aan de ene kant wordt aan uitgangspunt 3 (Minder schadelijke chemische productiemethoden) voldaan. De milieu-impact van de winning van fosfaat uit vivianiet is namelijk lager dan die van winning via het natte of thermale proces, omdat het fosfaat wordt herwonnen uit vivianiet in plaats van nieuw gewonnen uit erts. Als echter gekeken wordt naar de toevoeging van Fe3+ voor deze neerslag blijkt dat vivianiet ook nadelige gevolgen heeft voor het milieu op het gebied van ijzerwinning. Naast de hoeveelheid energie die nodig is, is de productie van ijzer namelijk ook vervuilend. Dit komt omdat er bij winning van ijzer uit erts naast gesmolten ijzer ook CO2 ontstaat. Per kg ijzer komt 1,85 kg CO2 vrij (Worldsteel, 2021). Daarnaast levert het winnen van erts en het vervoeren daarvan naar de hoogovens een bijdrage aan de CO2-uitstoot. Wat dit betreft voldoet vivianiet dus niet aan het derde uitgangspunt.
Het blijkt dat het probleem enkel verplaatst wordt van het fosfaaterts naar het ijzererts wanneer hieruit gewonnen ijzer wordt gebruikt voor fosfaatherwinning. Om het probleem van de vervuilende — en veel energie eisende — ijzerwinning uit erts te verhelpen is het van belang om te kijken naar uitgangspunt 7 (Gebruik van hernieuwbare grondstoffen). Er wordt naast het verwijderen van fosfaat namelijk onderzoek gedaan naar het verwijderen van ijzer uit vivianiet om het opnieuw te gebruiken voor de neerslagreactie (Utilities, 2020). Hiervan zijn nog niet veel resultaten, maar dit zou de cyclus sluiten en het proces van de vorming van vivianiet verduurzamen. Daarnaast wordt daarmee beter aan de uitgangspunten 3 (Minder schadelijke chemische productiemethoden) en 6 (Energie-efficient ontwerpen) voldaan, aangezien er geen schadelijke en energie eisende productie van ijzer meer nodig is.
Chloor
Met het toevoegen van FeCl2 wordt naast ijzer ook chloor aan het afvalwater toegevoegd. In dit onderzoek is de hoeveelheid chloor dat bij vivianiet toegevoegd wordt niet groot. Daarom veroorzaakt chloor geen milieuproblemen (Lenntech, 2022).
Zware metalen
Verder wijst uitgangspunt 1 (Preventie) bij vivianiet op een duurzaam proces, waarbij het opruimen van ‘afvalnutriënten’ uit afvalwater ook nog eens versterkt wordt. Dit komt doordat de nutriënten uit afvalwater worden gebonden aan vivianiet, waarbij eutrofiëring wordt voorkomen. Er kunnen echter ook vervuilende stoffen aan vivianiet binden. Studies tonen aan dat zware metalen zoals zink, lood, chroom, magnaan en kobalt in afvalwater binden aan vivianiet, dat hierbij als reductor functioneert (Taylor & Boult, 2007; Zachara, Fredrickson, Smith, & Gassman, 2001). Dit wordt in deze studies gezien als voordeel, aangezien het wordt toegepast in AWZI’s om zware metalen uit het water te halen. In context van dit onderzoek is de binding van zware metalen echter ongunstig, want dit betekent dat vivianiet een schadelijke chemische stof zou kunnen worden in een AZWI. Dit voldoet niet aan uitgangspunt 4 (van minder schadelijke chemische stoffen). Wanneer zich geen zware metalen in afvalwater bevinden, kan vivianiet wel zuiver gevormd worden, waarbij de ijzer en fosfaat de groei van gewassen bevorderen (Yuan, Wang, Wang, & Li, 2021). Dan is er dus wel aan uitgangspunt 4 voldaan.
3.3 Discussie theoretische resultaten
De duurzaamheid van de grondstoffen en van het proces van struviet- en vivianietvorming worden vergeleken op basis van energieverbruik, economie en milieu-impact. Struviet en vivianiet zijn in het voorgaande in deze categoriën beoordeeld aan de hand van de uitgangspunten voor de Groene Chemie. Vervolgens worden de twee fosfaatzouten hieronder vergeleken op deze aspecten, waarbij ook de SDG’s van de VN worden betrokken.
3.3.1 Energie en economie
In het kader van energie- en economiegerelateerde duurzaamheid zijn het zevende SDG van de VN (Betaalbare, duurzame energie) en uitgangspunt 6 van de EPA (Energie-efficiënt ontwerpen) van belang. Beide richten ze zich namelijk op het belang van het beperken en verduurzamen van energieverbruik en kosten. Daarnaast is in het kader van energie en economie uitgangspunt 9 (Katalyse) belangrijk, aangezien de katalysator de hoeveelheid energie die nodig is vermindert.
Energie grondstofproductie en proces
Wanneer struviet en vivianiet vergeleken worden op basis van energieverbruik van de grondstofproductie, blijkt dat vivianietneerslag niet optimaal duurzaam is. De productie van ijzer als grondstof voor vivianietneerslag kost namelijk veel energie. Hiermee voldoet de ijzerproductie niet aan SDG 7 (Betaalbare, duurzame energie) en uitgangspunt 6 (Energie-efficiënt ontwerpen). Fosfaatherwinning via struviet verbruikt daarnaast minder energie dan via fosfaaterts, terwijl bij fosfaatherwinning via vivianiet het energieverbruik enkel verplaatst wordt van fosfaaterts naar het ijzererts. Wat betreft het energieverbruik voor de productie van de grondstoffen is struviet dus duurzamer dan vivianiet.
Als gekeken wordt naar de energie die nodig is bij het proces, speelt bij de neerslagreactie van struviet mengenergie een rol, terwijl de neerslagreactie van vivianiet energieneutraal is. In tegenstelling tot struviet is er bij vivianiet echter wel weer veel energie nodig om het uit afvalwater te verwijderen. Hiervoor moet namelijk een sterk magnetisch veld gemaakt worden voor langere tijd. Wat deze twee zaken betreft, is geen van beide fosfaatzouten dus duidelijk duurzamer.
Een ander energiepunt voor het proces heeft betrekking op het katalysatorgebruik. Voor optimale struvietneerslag moet de pH verhoogd worden naar 9. Hiervoor wordt NaOH toegevoegd, wat dus uiteindelijk functioneert als katalysator. Op dit punt lijkt struviet volgens uitgangspunt 9 een voordeel te hebben. Uit de literatuur blijkt echter dat het proces van vivianiet behalve het toevoegen van Fe3+ geen aanpassingen in de omstandigheden vereist zoals die in afvalwater al zijn. De pH hoeft dus niet aangepast te worden en NaOH als katalysator is niet nodig. Vivianiet is op punt 9 dus eigenlijk beter, aangezien er helemaal niets nodig is in katalysevorm. Ondanks dat zou het natuurlijk kunnen dat de neerslagreactie van vivivaniet met een katalysator beter verloopt, maar daarvoor zou vervolgonderzoek nodig zijn. Zie hiervoor het kopje ‘Vervolgonderzoek’. Voor nu is vivianiet echter in deze context met energieverbruik voor pH-waarden duurzamer dan struviet.
Wanneer alles met betrekking tot het energieverbruik opgeteld wordt, blijkt dat momenteel geen van de fosfaatzouten duurzamer is.
Economie grondstofproductie en proces
Wanneer gekeken wordt naar de economische duurzaamheid van de grondstoffen voor struviet en vivianiet, blijkt uit de literatuur dat de productie van magnesium voor struvietneerslag hoge kosten met zich meebrengt. Deze kosten zijn nadelig voor de duurzaamheid volgens SDG 7 en uitgangspunt 6. Verder is de marktprijs van struviet is €500 per ton en die van vivianiet €
10.000 per ton: de productie van vivianiet brengt momenteel dus 20 keer zoveel op als die van struviet (Wu et al., 2019). Deze waardes kunnen echter in de toekomst veranderen als fosfaatverwijdering van vivianiet op grotere schaal zou worden toegepast. Economisch gezien is vivianiet dus aantrekkelijker dan struviet: er kan met vivianiet meer winst gemaakt worden.
3.3.2 Milieu
In het kader van milieu-impact zijn de uitgangspunten 1 (Preventie), 3 (Minder schadelijke productiemethoden), 4 (Ontwikkelen van minder schadelijke chemische stoffen), 7 (Gebruik van hernieuwbare grondstoffen), 10 (Ontwerpen met het oog op afbraak) en SDG 12 (Verantwoorde consumptie en productie), 13 (Klimaatactie), 14 (Leven in het water) en 15 (Leven op het land).
Wanneer gekeken wordt naar de impact van de fosfaatzouten struviet en vivianiet op het milieu, hebben beide fosfaatzouten minder impact dan het alternatief: het natte of thermale proces via fosfaaterts. Op dit punt is dus voldaan aan uitgangspunt 3 voor beide fosfaatzouten. Struviet en vivianiet kunnen echter wel worden vergeleken op dit punt: is struviet of vivianiet duurzamer wat betreft de grondstoffen en het proces?
Milieu-impact grondstoffen
Voor beide fosfaatzouten speelt de pH-waarde geen rol in milieu-impact. Voor vivianiet hoeven er geen aanpassingen gemaakt worden, aangezien voor vivianietneerslag een neutrale pH nodig is. Voor struviet moet NaOH toegevoegd worden voor het verhogen van de pH, maar kan NaOH hergebruikt worden. Op dit gebied voldoet struvietvorming dus aan uitgangspunt 7.
Ten tweede blijkt uit de literatuur dat voor de productie en het vervoer van ijzer voor vivianietneerslag CO2 wordt uitgestoten. Bij de productie van magnesium voor struvietneerslag is dit enkel zo voor vervoer. Deze CO2-uitstoot voldoet niet aan het dertiende SDG en moet ook vermeden worden met oog op het derde uitgangspunt. Aangezien ijzer meer CO2-uitstoot heeft dan magnesium, is vivianiet op dit punt minder duurzaam.
Wat betreft de milieu-impact van de grondstoffen heeft struviet dus een duurzamer profiel.
Milieu-impact proces
Wanneer gekeken wordt naar de invloed op het milieu van de struviet- en vivianietneerslag, is ten eerste een voordeel van beide fosfaatzouten dat ‘afvalnutriënten’ worden verwijderd uit afvalwater door binding met struviet of vivianiet. Deze verwijdering helpt mee om eutrofiëring van oppervlaktewater, waarin afvalwater geloosd wordt, te voorkomen. De neerslag van beide fosfaatzouten is dus overeenstemmend met uitgangspunt 1 en SDG 14 en 15. Op dit punt heeft struvietneerslag een bijkomend voordeel ten opzichte van vivianietneerslag, doordat het met één proces twee vervuilende nutriënten tegelijkertijd uit het afvalwater haalt. Naast fosfaat haalt struviet door neer te slaan namelijk ook ammonium uit het afvalwater, terwijl vivianiet op die manier alleen fosfaat uit het water haalt.
Door de binding met deze nutriënten kunnen struviet en vivianiet gebruikt worden als kunstmest, aangezien de bestandsdelen van deze fosfaatzouten plantengroei bevorderen. In dit kader speelt de zuiverheid van struviet en vivianiet echter ook een rol in de beoordeling van de duurzaamheid. Struviet en vivianiet kunnen namelijk respectievelijk ook medicijnen of zware metalen binden uit afvalwater. Struviet en vivianiet kunnen dus beide stoffen bevatten die nadelige gevolgen hebben voor het milieu. De impact van deze stoffen hangt wel af van de concentratie waarmee ze in het afvalwater en daarmee in de fosfaatzouten aanwezig zijn. Met het binden van vervuilende stoffen aan struviet en vivianiet zouden beide fosfaatzouten dus niet aan uitgangspunt 4 voldoen. Wat betreft zuiverheid kunnen struviet en vivianiet dus beide een gevaar vormen in bijvoorbeeld kunstmesttoepassing.
Verder voldoen struviet en vivianiet aan punt 10 en SDG 12, 14 en 15, aangezien beide producten bioafbreekbaar zijn en gebruikt worden in kunstmest. De ontwikkeling van fosfaatherwinning uit struviet lijkt echter verder gevorderd te zijn dan die uit vivianiet, aangezien SusPhos bezig is met het vormen van bioafbreekbare fosfaatproducten. Uiteindelijk kan dus gezegd worden dat struviet met betrekking tot de milieu-impact een duurzamer proces is dan vivianiet.
3.3.3 Toekomst: gebruik van hernieuwbare grondstoffen
Bij het analyseren van de duurzaamheid van struviet en vivianiet aan de hand van energieverbruik, economie en milieu-impact is het ook van belang om mogelijke toekomstige ontwikkelingen mee te nemen. Met name het zevende uitgangspunt en SDG 12 zijn hierbij van belang.
Er wordt de laatste tijd namelijk onderzoek gedaan naar het verwijderen van ijzer uit vivianiet en magnesium uit struviet om het opnieuw te gebruiken voor de neerslagreactie (Utilities, 2020). NaOH wordt al hergebruikt. Zie voor de gesloten fosforcyclus figuur 3.2. Door hergebruik van het ijzer en magnesium is geen productie van deze grondstoffen meer nodig. Hierdoor vervallen ten eerste de nadelen verbonden aan het hoge energieverbruik voor ijzerproductie en de hoge kosten voor magnesiumproductie. Er zou dan bij beide fosfaatzouten voldaan zijn aan uitgangspunt 6 en SGD 7.
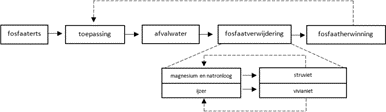
Figuur 3.2. Schematische representatie van de gesloten fosforcyclus.
Daarnaast betekent hergebruik dat het nadeel van de CO2- uitstoot voor beide fosfaatzouten vervalt. Daarmee zijn ze dan dus wel duurzaam volgens punt 3. Bij struviet wordt magnesium al hergebruikt op kleine schaal (VNCI, 2021), bij vivianiet is hier nog geen informatie over. Dit betekent dat struviet al verder is op het gebied van uitgangspunt 3 en 7. Het is dus waarschijnlijk dat magnesiumhergebruik eerder zal worden geïntroduceerd op grote schaal, wat struviet dus nu aantrekkelijker maakt voor duurzaamheidsoverwegingen.
Wanneer het hergebruik van grondstoffen echter in de toekomst op grote schaal wordt ingevoerd voor beide fosfaatzouten zal vivianiet als duurzamer proces uit de verf komen. Ondanks dat vivianiet dan gelijk scoort met struviet op milieu-impact van grondstoffen en zelfs slechter scoort op milieu-impact van het proces, scoort het juist beter op energieverbruik en economie, waardoor het vivianiet duurzamer is.
4. Discussie
4.1 Duurzaamheid: efficiëntie, grondstoffen en proces
Uit ‘Discussie experimentele discussie’ blijkt dat de efficiëntie van struviet bij alle temperaturen groter is dan die van vivianiet, wat overeenkomt met de hypothese over de efficiëntie. Daarnaast komt deze efficiëntie overeen met de hypothese over de temperatuur, aangezien struviet bij 20 °C het hoogste rendement. De efficiëntie van vivianiet komt echter niet overeen met de hypothese over de temperatuur. De efficiëntie bij 20 °C valt bij vivianiet namelijk niet zoals verwacht tussen 70 °C en 90 °C. Dit resultaat lijkt een afwijking te zijn, die mogelijk door een niet helemaal juiste manier van filteren of onbedoelde oxidatie veroorzaakt is.
Uit ‘Discussie theoretische resultaten’ kan herleid worden dat struviet duurzamer is op het gebied van energieverbruik, economie en milieu-impact. Dit blijkt uit de gegevens dat op het gebied van energie geen van de fosfaatzouten duurzamer is, op het gebied van economie vivianiet duurzamer is en op gebied van milieu-impact struviet twee keer een duurzamer profiel heeft. In de toekomst verandert dit beeld en zal de optelsom an de drie aspecten juist naar vivianiet leiden. Zie voor een overzicht ook tabel 4.1.
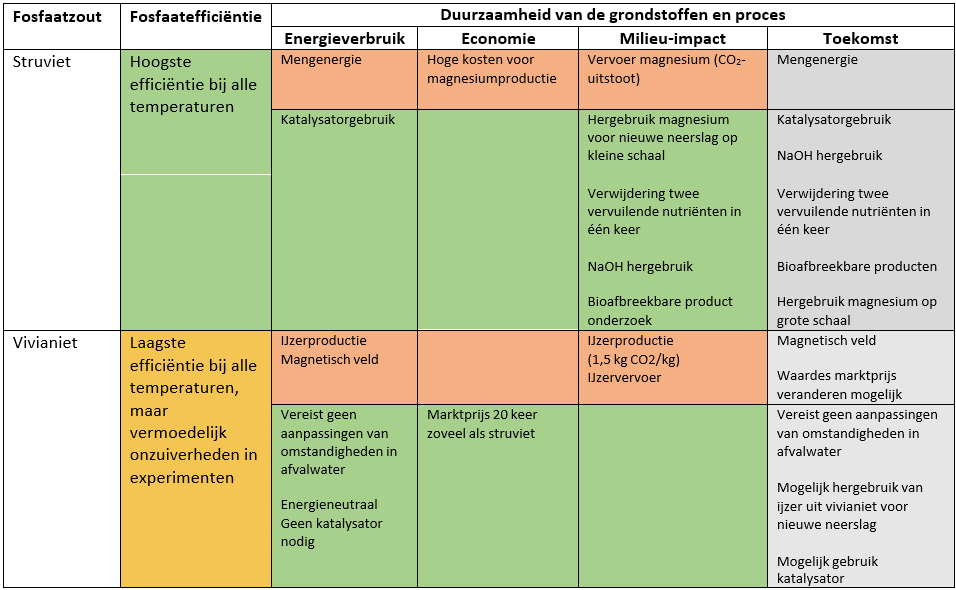
Tabel 4.1. Duurzaamheid van struviet en vivianiet
Als de efficiënte van fosfaatverwijdering gecombineerd wordt met de duurzaamheid op het gebied van energieverbruik, economie en milieu-impact blijkt dat struviet op beide gebieden duurzamer is dan vivianiet. Door de mogelijke afwijking zou vivianiet echter uiteindelijk toch beter kunnen zijn op efficiëntie. Dit zou gelijkspel betekenen voor de twee fosfaatzouten. Daarnaast kan vivianiet in de toekomst ook de betere optie worden op milieugerelateerd gebied. Het blijft dus de vraag welk van de fosfaatzouten op lange termijn beter is, maar aan de hand van dit onderzoek lijkt struviet het duurzaamst.
4.2 Verbeterpunten
- De afwijking van vivianiet bij 20 °C kan niet gecorrigeerd worden, aangezien het experiment niet in duplo of triplo is Daarvoor is een volgend onderzoek nodig, zodat gemiddelde waardes kunnen worden gebruikt, wat betrouwbaarder is dan een enkele meting.
- Er is per abuis 3 mL zuurstofarm demiwater te veel toegevoegd aan de oplossingen bij vivianiet. Daardoor was er uiteindelijk niet een 100 mL oplossing, maar een 103 mL De concentraties van de stoffen zijn hierdoor een klein beetje kleiner in de praktijk dan op papier. De hoeveelheid neerslag zal dus mogelijk iets lager zijn bij alle vivianietexperimenten. Bij volgende onderzoeken moet nauwkeuriger gewerkt worden.
4.3 Vervolgonderzoek
Naar aanleiding van dit onderzoek zijn enkele onderwerpen naar voren gekomen waarnaar onderzoek in de toekomst van belang is.
In een verbredend kader is het interessant om naar de gehele Life Cycle Analysis van fosfaat te kijken. In dit onderzoek is gekeken naar efficiëntie van verwijdering van fosfaat uit afvalwater, maar de stap om de cyclus te kunnen sluiten door PO 3- uit struviet al dan niet vivianiet te halen is minstens zo belangrijk. SusPhos (2022) en Wetsus (2022) zijn hier al mee bezig. De resultaten van efficiëntieonderzoek in deze richting kunnen verder bepalend zijn voor de voorkeur voor struviet of vivianiet.
Tevens is in dit kader onderzoek nodig naar de mogelijkheid tot het verwijderen van het ijzer uit vivianiet, waarna het opnieuw gebruikt kan worden voor de vorming van vivianiet. Dit zou ook weer een cyclus vormen, waardoor de niet-duurzame productie van ijzer onnodig wordt.
In het kader van verdiepend onderzoek is onderzoek met betrekking tot het belang van herhaald filteren interessant, vanwege de lagere massa neerslag van vivianiet na één keer filteren ten opzichte van de hogere massa neerslag van vivianiet na twee keer filteren. Wellicht zal op grote schaal ook herhaald moeten worden ‘gefilterd’ met een magneet om alle ijzerfosfaten uit het afvalwater te verwijderen. Hiervoor is echter techniekanalyse nodig op grote schaal, aangezien filterpapier uiteraard een materiaal in proef- en niet in praktijkcontext is.
Hieraan gerelateerd is vervolgonderzoek gericht op filterpapiergebruik in laboratoria relevant. Wellicht zijn bepaalde filterpapiersoorten niet geschikt voor Büchner-filtratie in verband met het tot twee keer toe scheuren van filterpapier in dit onderzoek.
Verder lijken de resultaten van het experiment bij 30 °C niet te passen in de lijn van het ongepubliceerde onderzoek van Beijer. In dit onderzoek lijkt een hogere temperatuur wel degelijk invloed te hebben op de neerslag, terwijl volgens Beijer hogere temperaturen geen invloed hebben op de neerslag. Om deze discrepantie verder uit te werken wordt vervolgonderzoek aangeraden waarin neerslag bij een groter scala aan temperaturen vergeleken wordt.
Daarnaast is vervolgonderzoek gericht op de mogelijkheid tot betere neerslagefficiëntie bij een kortere reactietijd interessant. In dit onderzoek is één reactietijd aangehouden, terwijl — zoals eerder vermeld — de studie van Buchynska (2017) vermeldt dat een kortere reactietijd (20 minuten) betere efficiënties realiseert (dan 60 minuten).
Tenslotte zou de neerslag van vivianiet mogelijk verbeterd kunnen worden met behulp van een katalysator. Voor struviet wordt deze al gebruikt in de vorm van NaOH, maar wellicht kan de vorming van vivianiet (en die van struviet op andere vlakken dan pH) nog verbeteren.
5. Conclusie
Terugwinning van fosfaat is belangrijk om de fosforcyclus te sluiten. Dit kan door afvalwater te zuiveren van fosfaat door de vorming en verwijdering van struviet en vivianiet. In dit onderzoek is gebleken dat de efficiëntie van struviet bij 0 °C, 20°C en 30 °C hoger is dan de efficiëntie van vivianiet. Daarnaast is struviet minder temperatuurafhankelijk. Wat efficiëntie van fosfaatverwijdering betreft, is struviet dus duurzamer dan vivianiet. Verder is gebleken dat struviet ook duurzamer is op het gebied van energieverbruik, economie en milieu-impact, maar in de toekomst zou vivianiet duurzamer kunnen worden. Door de afwijkende efficiëntie bij vivianiet bij 20 °C is het lastig te bepalen welk fosfaatzout betere fosfaatverwijdering biedt en minder temperatuurafhankelijk is. Door de mogelijke afwijking zou vivianiet uiteindelijk toch efficiënter kunnen zijn. Uiteindelijk zullen vervolgonderzoek en de mate van toekomstige ontwikkelingen bepalen of struviet of vivianiet een betere methode biedt.
Referenties
Ashley, K., Mavinic, D., & Koch, F. (2009). International Conference on Nutrient Recovery from Wastewater Streams (Vancouver, 2009). Water Intelligence Online, 8. https://doi.org/10.2166/9781780401805
Azam, H. M., Alam, S. T., Hasan, M., Yameogo, D. D. S., Kannan, D., Rahman, A., & Kwon, M. J. (2019). Phosphorous in the environment: characteristics with distribution and effects, removal mechanisms, treatment technologies, and factors affecting recovery as minerals in natural and engineered systems. Environmental Science and Pollution Research, Vol. 26, pp. 20183–20207. Springer Verlag. https://doi.org/10.1007/s11356-019-04732-y
Beijer, S., & Slootweg, J. C. (2021). Sustainable Phosphorus. In Encyclopedia of Inorganic and Bioinorganic Chemistry (pp. 1–26). Wiley. https://doi.org/10.1002/9781119951438.eibc2754
Buchynska, A. (2017). Phosphorus recovery through struvite precipitation: testing of parameters which enhance phosphorus recovery. Ås, Norway. Retrieved from http://hdl.handle.net/11250/2468301
Cao, J., Wu, Y., Zhao, J., Jin, S., Aleem, M., Zhang, Q., … Luo, J. (2019). Phosphorus recovery as vivianite from waste activated sludge via optimizing iron source and pH value during anaerobic fermentation. Bioresource Technology, 293. https://doi.org/10.1016/j.biortech.2019.122088
Desmidt, E., Ghyselbrecht, K., Zhang, Y., Pinoy, L., van der Bruggen, B., Verstraete, W., … Meesschaert, B. (2015). Global Phosphorus Scarcity and Full-Scale P-Recovery Techniques: A Review. Critical Reviews in Environmental Science and Technology, 45(4), 336–384. https://doi.org/10.1080/10643389.2013.866531
Environmental Protection Agency. (1980). Source category survey: thermal process phosphoric acid manufacturing industry. Retrieved from https://nepis.epa.gov/Exe/ZyPURL.cgi?Dockey=91010OY Y.txt
Environmental Protection Agency. (1998). Basics of Green Chemistry. Retrieved January 31, 2022, from https://www.epa.gov/greenchemistry/basics-green- chemistry#twelve
Environmental Protection Agency. (2021). Indicators: Phosphorus. Retrieved February 2, 2022, from https://www.epa.gov/national-aquatic-resource- surveys/indicators-phosphorus.
Fodoué, Y., Nguetnkam, J. P., Tchameni, R., Basga, S. D., & Penaye, J. (2015). Assessment of the Fertilizing effect of Vivianite on the Growth and yield of the Bean “‘phaseolus vulgaris’” on Oxisoils from Ngaoundere (Central North Cameroon). Retrieved from https://www.researchgate.net/publication/328042332
Foster, B. L., Tompkins, K. A., Rutherford, R. B., Zhang, H., Chu, E. Y., Fong, H., & Somerman, M. J. (2008). Phosphate: Known and potential roles during development and regeneration of teeth and supporting structures. Birth Defects Research Part C: Embryo Today: Reviews, 84(4), 281–314. https://doi.org/10.1002/bdrc.20136
Frederichs, T., von Dobeneck, T., Bleil, U., & Dekkers, M. J. (2003). Towards the identification of siderite, rhodochrosite, and vivianite in sediments by their low-temperature magnetic properties. Physics and Chemistry of the Earth, Parts A/B/C, 28(16–19), 669–679. https://doi.org/10.1016/S1474-7065(03)00121-9
Gantner, O., Schipper, W., & Weigand, J. J. (2014). Technological Use of Phosphorus: The Non-fertilizer, Non-feed, and Non- detergent Domain. In R. W. Scholz, A. H. Roy, F. S. Brand, T. Hellums, & A. E. Ulrich (Eds.), Sustainable Phosphorus Management – A Global Transdisciplinary Roadmap (pp. 237–242). Dordrecht: Springer. Retrieved from https://gnusha.org/~nmz787/pdf/Sustainable_Phosphor us_Management.pdf
Ghangrekar, M., Sathe, S., & Das, S. (2021). Bioenergy and Valuables Recovery During Wastewater Treatment Using Bio-Electrochemical Systems. Reference Module in Earth Systems and Environmental Sciences. https://doi.org/10.1016/B978-0-12-819727-1.00041-8
Henze, M., Harremoes, P., Arvin, E., & la Cour Jansen, J. (2001). Wastewater Treatment: Biological and Chemical Processes (3rd ed.). Springer.
Hofman, R., & van den Brand, T. (2020). Milieu-impact van NaOH en kalk(melk) in de drinkwaterzuivering. Retrieved January 26, 2022, from https://www.kwrwater.nl/projecten/milieu-impact-van- naoh-en-kalkmelk-in-de-drinkwaterzuivering/
Imran, B., Khan, S. J., Qazi, I. A., & Arshad, M. (2015). Removal and recovery of sodium hydroxide (NaOH) from industrial wastewater by two-stage diffusion dialysis (DD) and electrodialysis (ED) processes. New Pub: Balaban, 57(17), 7926–7932. https://doi.org/10.1080/19443994.2015.1048742
Isaac Asimov. (1974). Asimov on Chemistry. Oklahoma City: Mercury Press.
Jupp, A. R., Beijer, S., Narain, G. C., Schipper, W., & Slootweg, J.(2021). Phosphorus recovery and recycling – closing the loop. Chemical Society Reviews, 50(1), 87–101. https://doi.org/10.1039/D0CS01150A
Kabdaşlı, N., Parsons, S. A., & Tunay, O. (2006). Effect of major ions on induction time of struvite precipitation. Croatica Chemica Acta, 79, 243–251. Retrieved from https://hrcak.srce.hr/file/6800
Kataki, S., West, H., Clarke, M., & Baruah, D. C. (2016). Phosphorus recovery as struvite: Recent concerns for use of seed, alternative Mg source, nitrogen conservation and fertilizer potential. Resources, Conservation and Recycling, 107. https://doi.org/10.1016/j.resconrec.2015.12.009
Kemacheevakul, P., Otani, S., Matsuda, T., & Shimizu, Y. (2012). Occurrence of micro-organic pollutants on phosphorus recovery from urine. Water Science and Technology, 66(10), 2194–2201.
https://doi.org/10.2166/wst.2012.452
Koopmans, G., Chardon, W., Belder, P., & Groenenberg, B.-J. (2011). Verwijdering van fosfaat uit bodemwater met ijzerzand: de omhulde drain. Retrieved from https://edepot.wur.nl/212350
Korving, L. (2018). Fosfaat, van verwijdering naar terugwinning. Biowetenschappen En Maatschappij, 37(2), 75–77. Retrieved from https://www.biomaatschappij.nl/wp- content/uploads/2020/11/Afvalwater.pdf
Lapota, D., Duckworth, D., & Word, J. (2000). Confounding Factors in Sediment Toxicology. Retrieved from https://clu- in.org/download/contaminantfocus/sediments/testing- sediments-confound.pdf
Lenntech. (2022). Chloor en water. Retrieved February 5, 2022, from https://www.lenntech.nl/elementen-en- water/chloor-en water.htm#:~:text=Chloor%20oftewel%20chloride%20is%20normaal,zelfs%20rond%2024%20g%2Fl
Liao, P. H., Wong, W. T., & Lo, K. v. (2005). Release of phosphorus from sewage sludge using microwave technology. Journal of Environmental Engineering and Science, 4(1). https://doi.org/10.1139/s04-056
Liu, X., Wen, G., Hu, Z., & Wang, J. (2018). Coupling effects of pH and Mg/P ratio on P recovery from anaerobic digester supernatant by struvite formation. Journal of Cleaner Production, 198, 633–641. https://doi.org/10.1016/j.jclepro.2018.07.073
McCammon, C. A., & Burns, R. G. (1980). The oxidation mechanism of vivianite as studies by Möessbauer spectroscopy . American Mineralogist, 65(3–4), 361–366. Retrieved from https://pubs.geoscienceworld.org/msa/ammin/article- abstract/65/3-4/361/41145/The-oxidation-mechanism- of-vivianite-as-studies-by?redirectedFrom=fulltext
Morgenschweis, C., Vergouwen, L., Schöll, L. van, & Leenen, I. (2015). Verkenning van de kwaliteit van struviet uit de communale afvalwaterketen. Retrieved from https://www.stowa.nl/sites/default/files/assets/PUBLICA TIES/Publicaties%202015/STOWA%202015-34.pdf
Morse, G., Brett, S., Guy, J., & Lester, J. (1998). Review: Phosphorus removal and recovery technologies. The Science of The Total Environment, 212(1), 69–81. https://doi.org/10.1016/S0048-9697(97)00332-X
Muryanto, S. (2017). On precipitation of struvite (MgNH4PO4.6H2O). Journal of Science and Science Education, 1(2), 21–29. https://doi.org/10.24246/josse.v1i2p21-29
Nriagu, J. O. (1972). Stability of vivianite and ion-pair formation in the system fe3(PO4)2-H3PO4H3PO4-H2o. Geochimica et Cosmochimica Acta, 36(4), 459–470. https://doi.org/10.1016/0016-7037(72)90035-X
NWO. (2021). Struvite recycling to the next level thanks to Gouden KIEM. Retrieved February 2, 2022, from https://www.nwo.nl/en/news/struvite-recycling-next- level-thanks-gouden-kiem
Prot, T., Korving, L., Dugulan, A. I., Goubitz, K., & van Loosdrecht, C. M. (2021). Vivianite scaling in wastewater treatment plants: Occurrence, formation mechanisms and mitigation solutions. Water Research, 197. https://doi.org/10.1016/j.watres.2021.117045
Prot, T., Nguyen, V. H., Wilfert, P., Dugulan, A. I., Goubitz, K., de Ridder, D. J., … van Loosdrecht, M. C. M. (2019). Magnetic separation and characterization of vivianite from digested sewage sludge. Separation and Purification Technology, 224, 564–579. https://doi.org/10.1016/j.seppur.2019.05.057
Rothe, M., Kleeberg, A., & Hupfer, M. (2016). The occurrence, identification and environmental relevance of vivianite in waterlogged soils and aquatic sediments. Earth-Science Reviews, 158, 51–64. https://doi.org/10.1016/j.earscirev.2016.04.008
Ruttenberg, K. C. (2014). The Global Phosphorus Cycle. Treatise on Geochemistry: Second Edition, 10, 499–558. https://doi.org/10.1016/B978-0-08-095975-7.00813-5
Rychkov, V. N., Kirillov, E. V., Kirillov, S. V., Semenishchev, V. S., Bunkov, G. M., Botalov, M. S., … Malyshev, A. S. (2018). Recovery of rare earth elements from phosphogypsum. Journal of Cleaner Production, 196. https://doi.org/10.1016/j.jclepro.2018.06.114
Santa Cruz Biotechnology. (2010). Material Safety Data Sheet – Aluminium Phosphate. Retrieved from https://datasheets.scbt.com/sc-291880.pdf
Siciliano, A., Limonti, C., Curcio, G. M., & Molinari, R. (2020). Advances in Struvite Precipitation Technologies for Nutrients Removal and Recovery from Aqueous Waste and Wastewater. Sustainability, 12(18), 7538. https://doi.org/10.3390/su12187538
Solomon, S., Plattner, G.-K., Knutti, R., & Friedlingstein, P. (2009). Irreversible climate change due to carbon dioxide emissions. Proceedings of the National Academy of Sciences of the United States of America, 106(6), 1704– 1709. https://doi.org/10.1073/pnas.0812721106
Stuart Chapin, F., Matson, P. A., & Vitousek, P. M. (2012). Principles of terrestrial ecosystem ecology. Principles of Terrestrial Ecosystem Ecology, 1–529. https://doi.org/10.1007/978-1-4419-9504-9
SusPhos. (2022). SusPhos – Use smart chemistry for a better world. Retrieved January 27, 2022, from https://www.susphos.com
Szymańska, M., Szara, E., Wąs, A., Sosulski, T., van Pruissen, G., & Cornelissen, R. (2019). Struvite—An Innovative Fertilizer from Anaerobic Digestate Produced in a Bio-Refinery. Energies, 12(2), 296. https://doi.org/10.3390/en12020296
Talboys, P. J., Heppell, J., Roose, T., Healey, J. R., Jones, D. L., & Withers, P. J. A. (2016). Struvite: a slow-release fertiliser for sustainable phosphorus management? Plant and Soil, 401(1–2), 109–123. https://doi.org/10.1007/s11104-015-2747-3
Taylor, K. G., & Boult, S. (2007). The role of grain dissolution and diagenetic mineral precipitation in the cycling of metals and phosphorus: A study of a contaminated urban freshwater sediment. Applied Geochemistry, 22(7), 1344–1358. https://doi.org/10.1016/J.APGEOCHEM.2007.01.008
UN-DESA. (2015). Transforming our world: The 2030 Agenda for Sustainable Development. United Nations. Retrieved from https://stg-wedocs.unep.org/bitstream/handle/20 500.11822/11125/unepswiosm1inf7sdg.pdf?sequence=1
UN-DESA. (2022). Home | Sustainable Development. Retrieved February 5, 2022, from https://sdgs.un.org/
US Department of Energy. (1999). Caustic Recycle. Retrieved from https://kbem.org/DOEKMDocuments/ITSR/Tank/Caustic_ Recycle.pdf
Utilities. (2020, January 21). Vivianiet volgende stap in urban mining. Retrieved January 26, 2022, from https://utilities.nl/vivianiet-volgende-stap-in-urban- mining/
van der Grinten, E., & Spijker, J. (2017). Medicijnresten, pathogenen en antibioticaresistentie in struviet uit Nederlands huishoudelijk afvalwater. https://doi.org/10.21945/RIVM-2017-0144
Versteegh, J., Morgenstern, P., & te Biesebeek, J. (2004). De Drinkwaterkwaliteit in Nederland van 1992 tot 2002 – Een overzicht van tien jaar kwaliteitsbewaking. Bilthoven. Retrieved from https://www.rivm.nl/bibliotheek/rapporten/734301024. pdf
ViviMag. (2022). About. Retrieved February 1, 2022, from https://www.vivimag.nl/about
VNCI. (2021). Recycling: SusPhos maakt de fosfaatcirkel rond. Retrieved February 3, 2022, from https://vnci.nl/chemie- magazine/actueel/artikel?newsitemid=5861638144
Wang, Y., Gao, P., Fan, M., & Jin, H. (2011). Preliminary Study of Purification for Livestock Wastewater of Immobilized Microcystis Aeruginosa. Procedia Environmental Sciences, 11, 1316–1321. https://doi.org/10.1016/j.proenv.2011.12.197
Wetsus. (2021). ViviMag. Retrieved December 10, 2021, from https://www.wetsus.nl/european-projects/vivimag/
Wetsus. (2022). Phosphate recovery – Wetsus. Retrieved January 27, 2022, from https://www.wetsus.nl/research- themes/phosphate-recovery/
Wilfert, P., Dugulan, A. I., Goubitz, K., Korving, L., Witkamp, G. J., & van Loosdrecht, M. C. M. (2018). Vivianite as the main phosphate mineral in digested sewage sludge and its role for phosphate recovery. Water Research, 144, 312–321. https://doi.org/10.1016/j.watres.2018.07.020
Worldsteel. (2021). Climate change and the production of iron and steel. Retrieved from http://worldsteel.org/wp- content/uploads/Climate-change-and-the-production-of- iron-and-steel.pdf
Wu, Y., Luo, J., Zhang, Q., Aleem, M., Fang, F., Xue, Z., & Cao, J. (2019). Potentials and challenges of phosphorus recovery as vivianite from wastewater: A review. Chemosphere, 226, 246–258. https://doi.org/10.1016/j.chemosphere.2019.03.138
Yang, Y., Raipala, K., & Holappa, L. (2014). Ironmaking. In Treatise on Process Metallurgy (Vol. 3, pp. 2–88). Elsevier. https://doi.org/10.1016/B978-0-08-096988-6.00017-1
Ye, Z., Shen, Y., Ye, X., Zhang, Z., Chen, S., & Shi, J. (2014).
Phosphorus recovery from wastewater by struvite crystallization: Property of aggregates. Journal of Environmental Sciences, 26(5), 991–1000. https://doi.org/10.1016/S1001-0742(13)60536-7
Ye, Z.-L., Deng, Y., Lou, Y., Ye, X., Zhang, J., & Chen, S. (2017).
Adsorption behavior of tetracyclines by struvite particles in the process of phosphorus recovery from synthetic swine wastewater. Chemical Engineering Journal, 313, 1633–1638. https://doi.org/10.1016/j.cej.2016.11.062
Yuan, Q., Wang, S., Wang, X., & Li, N. (2021). Biosynthesis of vivianite from microbial extracellular electron transfer and environmental application. Science of The Total Environment, 762, 143076. https://doi.org/10.1016/J.SCITOTENV.2020.143076
Zachara, J. M., Fredrickson, J. K., Smith, S. C., & Gassman, P. L. (2001). Solubilization of Fe(III) oxide-bound trace metals by a dissimilatory Fe(III) reducing bacterium. Geochimica et Cosmochimica Acta, 65(1), 75–93. https://doi.org/10.1016/S0016-7037(00)00500-7
Zhang, X. (2012). Factors Influencing Iron Reduction–Induced Phosphorus Precipitation. Environmental Engineering Science, 29(6), 511–519. https://doi.org/10.1089/ees.2011.0114