
C3 JongerenCommunicatie
Aangemaakte reacties
-
AuteurBerichten
-
10 augustus 2023 om 10:05 In reactie op: Samenstelling en verhouding van esters in citrusvruchten #158724
C3 JongerenCommunicatie
SleutelbeheerderBeste Anissa,
De vraagbaak is eigenlijk gesloten in de zomer, dus er zijn geen experts aanwezig om je vraag te beantwoorden. Maar gelukkig kunnen we je wel helpen. Het is geen volldige bron en ook niet het volledige antwoord op je vraag, maar op wikipedia in het Engels is een lijst met esters en welke geur ze hebben terug te vinden:
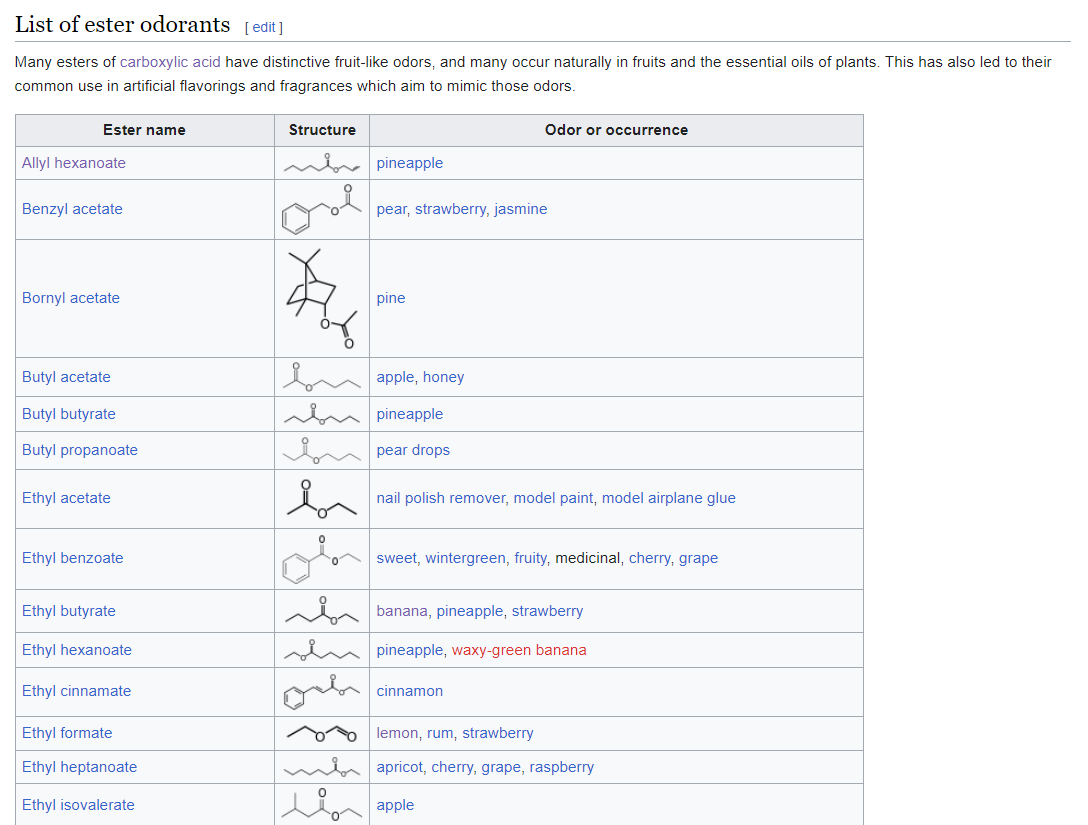
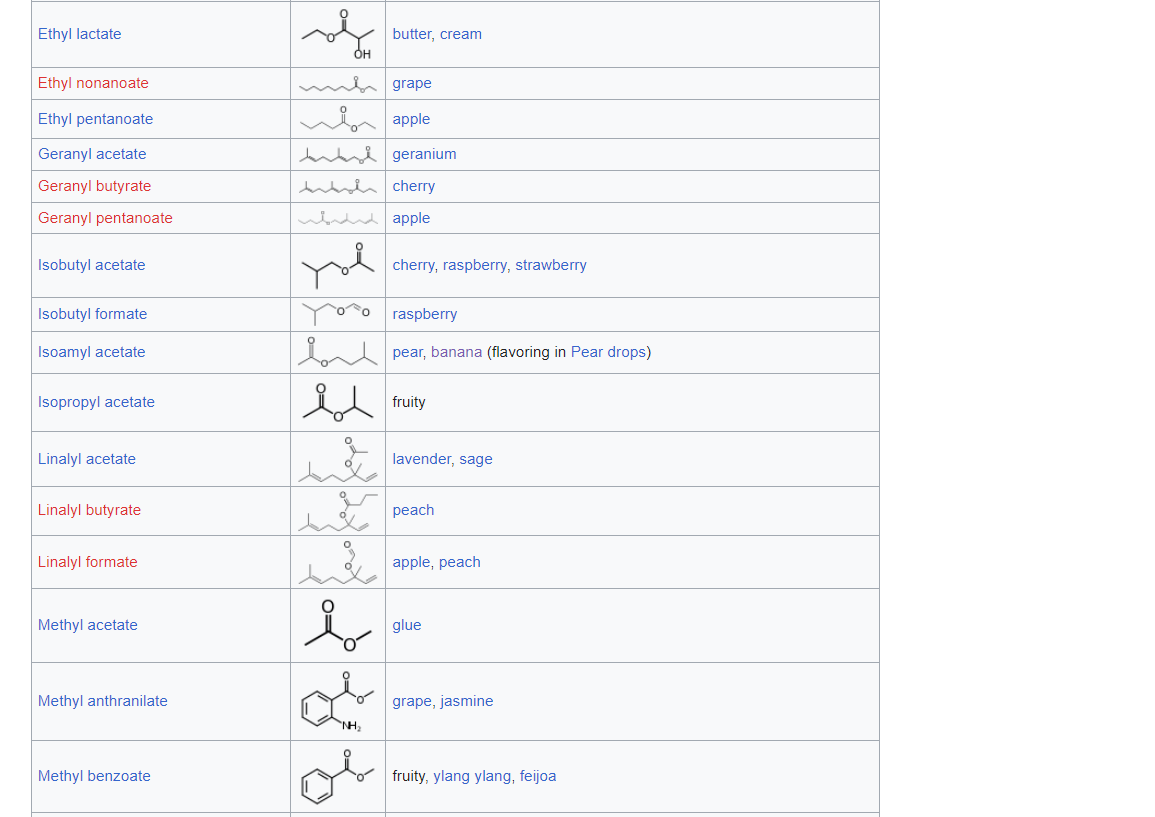
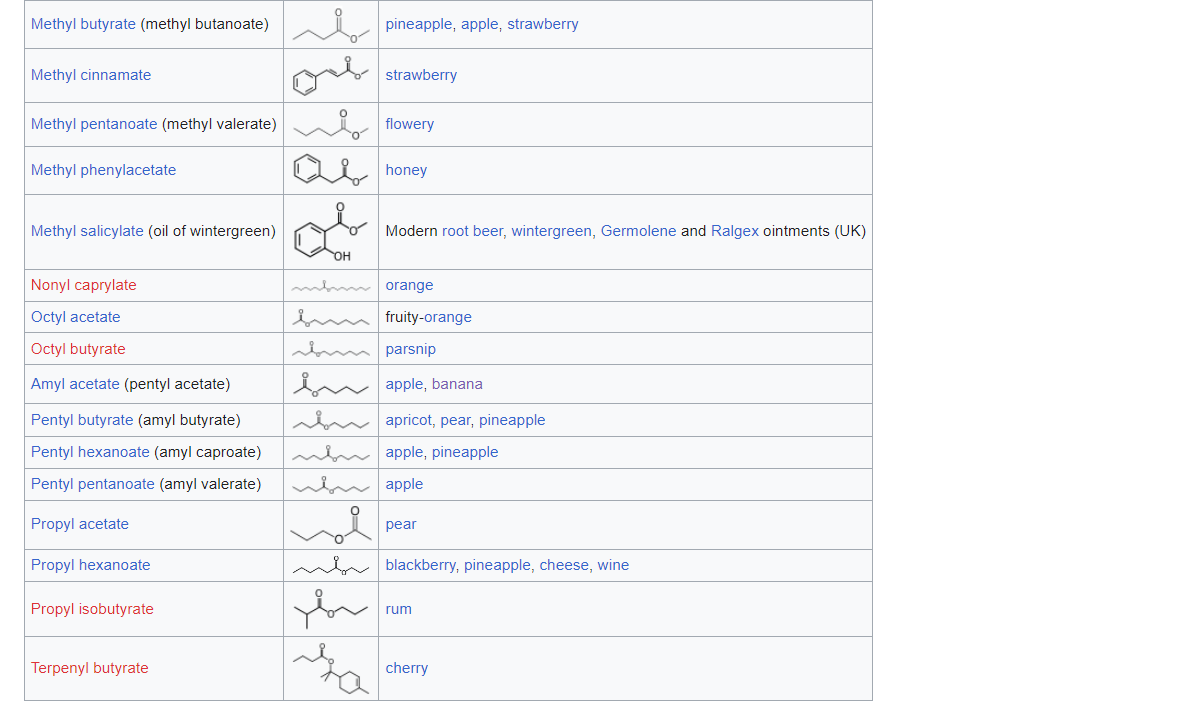
Bron: https://en.wikipedia.org/wiki/List_of_esters
of kijk in deze infographic (ook in het Engels) https://jameskennedymonash.wordpress.com/2013/12/13/infographic-table-of-esters-and-their-smells/
Ik hoop dat je hier wat verder mee kunt. En anders ben je welkom om in september je vraag opnieuw te stellen, dan zijn onze experts weer aanwezig die je verder kunnen helpen.
Met vriendelijke groet,
Team C3
18 juli 2023 om 12:27 In reactie op: Berekenen van drukstijging in stilstaande tank met vloeibaar propaan #158482C3 JongerenCommunicatie
SleutelbeheerderBeste Stijn,
In verband met de zomervakantie is de vraagbaak gesloten en zijn er op dit moment geen experts aanwezig om je vraag te beantwoorden. Vanaf 4 september zijn we open en kun je weer alle vragen stellen.
Met vriendelijke groet,
Team C3
C3 JongerenCommunicatie
SleutelbeheerderBeste Julius,
Door het kopiëren van de tekst uit je verslag komen er tekens (html code) mee die je in eerste instantie niet ziet bij het stellen van de vraag, maar wel getoond worden hierboven. Ik heb de meeste tekens weg kunnen halen, maar ik zie dat je een tabel hebt geplakt en deze kan niet getoond worden. Kun je je resultaten nogmaals sturen maar dan zelf ingetypt en niet geknipt en geplakt? Dan komt de htmlcode niet mee.
Met vriendelijke groet,
Winnie (moderator)
C3 JongerenCommunicatie
SleutelbeheerderHoi Theo!
Hoe dit kan is makkelijker te begrijpen als je bedenkt wat een katalysator doet met de energie tijdens het lopen van de reactie.
De ene kant op gaat de energie omhoog van E(1) via een berg met totale hoogte E(x) en dan naar beneden naar E(2). En de andere kant op dus van E(2) via dezelfde berg E(x) en dan terug naar beneden naar E(1). Een reactie loopt traag als E(x) veel hoger is dan de begintoestand, dus als E(x)-E(1) groot is voor de heengaande reactie, en E(x)-E(2) voor de teruggaande reactie.
Wat de katalysator doet is E(x) lager maken, zeg tot E(y). Daarmee wordt de berg vanaf de ene kant lager (E(y)-E(1) is kleiner dan E(x)-E(1)) maar vanaf de andere kant wordt de berg precies even veel lager! (E(y)-E(2) is kleiner dan E(x)-E(2)). En dat zorgt ervoor dat de versnelling beide kanten op precies even groot is.
(zie bijgesloten afbeelding)
Groet, Rob
C3 JongerenCommunicatie
SleutelbeheerderHallo Tom,
Je weet natuurlijk dat er voor redoxreacties in BINAS 48 halfreacties staan. Je moet met de beschikbare deeltjes(stoffen) de halfreactie vinden van de Reductor en die van de Oxidator. Daarbij zoek je naar de sterkste reductor, die mogelijk is en naar de sterkste oxidator.
Punt is natuurlijk dat je de beschikbare stoffen zo moet schrijven zoals de deeltjes in de oplossing.
Bijvoorbeeld, zwavelzuur is een sterk zuur en opgelost in water altijd aanwezig als H+(aq) en SO4 2-(aq). Als je het laat staan als H2SO4 zul je de bewuste halfreactie in tabel 48 niet vinden.
Probeer dit eens en laat weten of het je lukt.Succes en groet,
Jan Wim Peters
C3 JongerenCommunicatie
SleutelbeheerderBeste Nick,
Vanwege technische problemen is het antwoord op jouw vraag niet weergegeven. Onderstaand alsnog. Excuus voor het ongemak.
Groet, Susanne (moderator)
Hallo Nick,
Ik begrijp dat jouw vraag alleen gaat over het opstellen van de reactievergelijking.
Als je moeite hebt het hele proces in één reactievergelijking te schrijven, doe het dan in aparte stappen. Deze stappen staan in de tekst genoemd: je krijgt dan twee reactievergelijkingen. Als je die twee vergelijkingen samen neemt (weet je hoe je dat moet doen?), moet je uitkomen op de reactievergelijking die je zelf al als antwoord had genoemd.
Groeten,
Wim Wessel
C3 JongerenCommunicatie
SleutelbeheerderBeste Nick,
Vanwege technische problemen is onderstaand antwoord niet weergegeven. Excuus voor de vertraging.
Groet, Susanne (moderator)
Het lijkt erop dat mijn eerste antwoord niet goed is doorgekomen, dus ik probeer het nog eens.
Als eerste: is het je opgevallen dat je een neerslagreactie krijgt als je deze twee oplossingen bij elkaar voegt?
Wat de opgave nu van je vraagt: ga eerst na welke ionen je aan het begin hebt: soorten en hoeveelheden (in mol of in mmol).
Kijk dan welke ionen uit de oplossing verdwijnen door de neerslagreactie en hoeveel.
Je weet dan welke ionen er nog over zijn. Je kunt dan met de hoeveelheden en het totale (!) volume de concentraties in mol/ L of mmol/ mL (is hier handiger) berekenen.Ik hoop dat je hiermee wat kunt.
Groeten,
Wim Wessel
C3 JongerenCommunicatie
SleutelbeheerderBeste Mirthe,
Bekijk eens de onderstaande site:
https://www.aanpakstikstof.nl/het-stikstofprobleemHet bevat uitleg met ook een duidelijke video.
Als je nog vervolgvragen hebt, dan verneem ik die wel.
Groeten,
Docent Dick
C3 JongerenCommunicatie
SleutelbeheerderBeste Anna,
Bekijk de onderstaande site eens:
https://nl.wikipedia.org/wiki/Akkoord_van_ParijsMocht je nog vervolgvragen hebben dan verneem ik die wel.
Groeten,
Docent Dick
C3 JongerenCommunicatie
SleutelbeheerderHoi,
Je berekening klopt helemaal. Goed gedaan! Het enige wat nu nog niet goed is, is de significantie. Als de pH met één cijfer achter de komma wordt gegeven, dient je eindantwoord ook slechts één cijfer te bevatten.
Groetjes,
Loes-
Deze reactie is gewijzigd 2 jaren, 6 maanden geleden door
C3 JongerenCommunicatie.
C3 JongerenCommunicatie
SleutelbeheerderBeste Siemen,
Bedankt voor je vraag! Om meteen eerlijk te zijn, dit onderwerp is niet onze specialiteit, maar we hebben wel intern overlegd over welke opties mogelijk zijn om aluminium met een andere laag aluminium te bekleden. Daaruit zijn de volgende opties gekomen:
– Lassen
Dit is zeker een mogelijke optie alleen is het wel lastig onder andere doordat aluminium erg reactief is t.o.v. zuurstof zoals je hebt aangegeven. Lassen kost veel werk en de lagen zijn vervolgens moeilijk glad te krijgen.– Elektrochemie
Inderdaad kan je dit niet op waterbasis doen. Je zult dit in een gesmolten zoutoplossing moeten uitvoeren met als consequentie dat je tegelijkertijd ook de aluminiumdelen smelt. Deze optie is dus wellicht niet verstandig.– Poedercoaten
Bij deze techniek wordt elektrisch geladen poeder gespoten op een oppervlakte waaraan het poeder vervolgens hecht. Deze methode wordt echter gebruikt als je een hele dunne laag wilt aanbrengen en we weten niet of dit past binnen jouw onderzoek. Als je geïnteresseerd bent, raad ik je aan om deze link te bekijken: https://coating.nl/aluminium-coating/-MMA lijm
Je kan aluminium platen ook aan elkaar lijmen met epoxylijm, of in dit geval MMA lijm (de lagen plakken aan elkaar vast doordat MMA polymeriseert en crosslinks vormt met de twee lagen). Dit is een mogelijk alternatief en meer informatie kan je vinden op https://www.comhan.com/nl/blog/aluminium-bewerken-behandelen/aluminium-lijmen-wat-zijn-de-voordelen-Vacuüm depositie
Afhankelijk van wat de mogelijkheden zijn, zou je de twee lagen aan elkaar kunnen krijgen door ze atoom-voor-atoom te binden. Dit vindt plaats onder vacuüm en vereist de nodige instrumenten. Wij hebben er echter geen ervaring mee.We hopen dat je met deze opties wat verder kunt komen! Laat het vooral weten als we je verder kunnen helpen.
Groetjes,
Siebe
C3 JongerenCommunicatie
SleutelbeheerderBeste Wim,
Het zou bij 20ºC vloeibaar kunnen zijn de stof niet 100% zuiver is, als het opgelost is in een andere stof of/en als er hulpstoffen bij zitten.
Over de gezondheidsrisico’s kunnen en willen we geen uitspraken doen. Wellicht zou je daarvoor contact met een adviesbureau voor gevaarlijke stoffen kunnen opnemen. Wij komen niet verder dan de International Chemical Safety Card te vinden op:
https://www.ilo.org/dyn/icsc/showcard.display?p_lang=en&p_card_id=1111Met vriendelijke groet,
Jan-Hein(Excuus voor de late reactie maar een eerdere reactie was niet geregistreerd)
C3 JongerenCommunicatie
SleutelbeheerderHelemaal goed.
Om het hele proces goed te begrijpen wil ik je ook vragen of je kunt bedenken waarom de oplossing moet worden aangezuurd met een overmaat zwavelzuur voordat de titratie kan plaatsvinden?
Blijkbaar is een aanzuring nodig om de juiste analyse met de titratie te kunnen doen.
Waarom leidt het NIET aanzuren van de oplossing tot een onjuiste bepaling van het sulfiet gehalte?C3 JongerenCommunicatie
SleutelbeheerderHallo Josephine, laat ik proberen te helpen.
Je hebt de juiste halfreacties genomen en totaalreactie opgesteld.
Zoals je dus ziet wordt het sulfiet ion omgezet in een sulfaat-ion bij de redox-titratie.
Maar sulfiet kan alleen worden omgezet door I_2 als het ook in deze losse ion-vorm in de witte wijn aanwezig is.
Sulfiet in witte wijn is voor een groot gedeelte gebonden aan andere stoffen, zoals o.a. aldehydes.
Wat zou dan de functie van de overmaat OH^- ionen zijn die als voorbereiding voor de titratie worden toegevoegd?
Kan je ook bedenken waarom er direct vóór de titratie zwavelzuur moet worden toegevoegd?-
Deze reactie is gewijzigd 2 jaren, 6 maanden geleden door
C3 JongerenCommunicatie.
C3 JongerenCommunicatie
SleutelbeheerderBeste Tim,
van bioafval naar biogas is een ingewikkeld proces, daarbij is het niet zo dat alleen suikers gevormd worden en dat die vergisten tot biogas (methaan en koolstofdioxide).
In de attachfile heb ik de tekst van de link https://www.zerofoss.nl/index.php/zerofoss-producten/biogas toegevoegd.bioafval >hydrolyse>verzuring>azijnzuurvorming>biogasvorming>zuiveren>biogas
Met vriendelijke groet,
Docent Dick
-
Deze reactie is gewijzigd 2 jaren, 6 maanden geleden door
-
AuteurBerichten
