Dit zijn opgaven 9 t/m 17 uit het eindexamen scheikunde havo 2021 tijdvak 1.
Wil je bij opgave 1 starten? Ga dan naar het begin van dit examen.
Lithium-ionbatterij
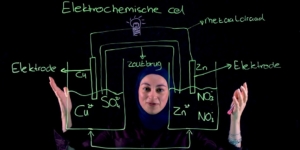
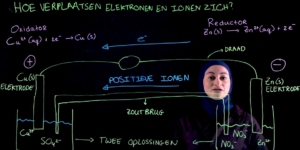
In veel mobiele telefoons zit een lithium-ionbatterij. Deze batterijen zijn licht, kunnen veel energie leveren en zijn snel op te laden. Het basisontwerp van een lithium-ionbatterij is in figuur 1 schematisch weergegeven.

Elektrode A bevat onder andere het metaal lithium (Li). Elektrode B bevat Li+-ionen. Tussen beide elektroden bevindt zich een elektrolyt, dat bestaat uit een polymeer waarin zich een vloeibaar lithiumzout bevindt. Een veelgebruikt polymeer is PEO. De formule van PEO is (CH2CH2O)n.
In figuur 2 is een vergroting van het elektrolyt schematisch weergegeven. Hierin is te zien hoe een Li+-ion van polymeerketen naar polymeerketen wordt doorgegeven, doordat telkens een ander groepje O-atomen het Li+-ion bindt. De binding komt tot stand doordat de O-atomen in PEO enigszins negatief geladen zijn. Dit is het gevolg van een polaire atoombinding tussen de C-atomen en de O-atomen in PEO. Tijdens de stroomlevering bewegen Li+-ionen van elektrode A naar elektrode B.

Ga naar de volgende opgaven van het eindexamen scheikunde havo 2021 tijdvak 1 deel 3.
Bron: examenblad.nl