De concentratie H3O+ kun je berekenen aan de hand van de gegeven pH. Gebruik hiervoor de formule [H+] =10 -pH
[H3O+] = 10-pH . Deze formule kun je terugvinden in Binas tabel 38A.
[H3O+] = 10-pH = 10-7,40 = 3,98 · 10-8 = 3,98 · 10-8
De Kz van NH3 is 6,3 · 10–11 (deze informatie is in de tekst gegeven)^.
De reactievergelijking is ~NH3 + H2O ⇌ ~NH2 + H3O+, uit de tekst is namelijk op te maken dat ~NH3+-groepen reageren en ~NH2 een reactieproduct is.
Vervolgens moet de formule voor de evenwichtsconstante worden opgesteld. Gebruik hiervoor a A+b B ⇌ c C+d D en K = ([C]c[D]d) / ([A]a[B]b). Deze formules kun je vinden in Binas tabel 37B.
Kz = [~NH2][H3O+]/[~NH3+] = 6,3 · 10-11
Kz = [~NH2] 3,98 · 10-8 / [~NH3+] = 6,3 · 10-11
[~NH2]/[~NH3+] = 1,58 · 10-3
Het percentage [~NH2] kun je berekenen door: Massapercentage = [(massa gevraagde stof) / (totale massa)] × 100%.
~NH2 = (1,582 · 10-3 / 1 + 1,58 · 10-3) x 100% = 0,16 (en dat is kleiner dan 2,0)
Aanvullende voorbeelden juiste berekeningen:
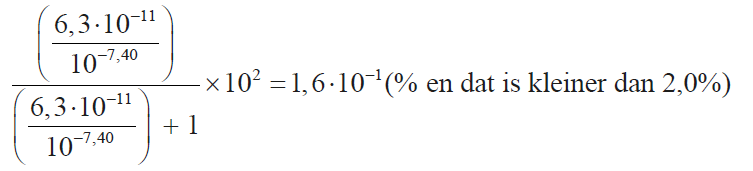

Toelichting puntenscore:
- Berekening van de [H3O+] = 1
- De evenwichtsvoorwaarde juist, eventueel reeds gedeeltelijk ingevuld = 1
- Uitwerken van de berekening tot bijvoorbeeld (eventueel impliciet)
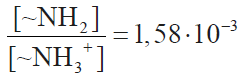 = 1
= 1
- Omrekening naar het percentage = 1