Geen zin om een filmpje te bekijken? Hieronder lees je de tekst:
Hoi, ik ben Lotte van de Sisters in Science en in dit filmpje ga ik jullie uitleggen wat er gebeurt tijdens het opladen van een elektrochemische cel.
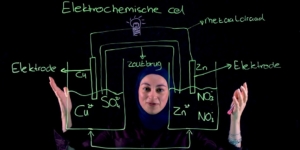
Maar om dat te kunnen doen moeten we natuurlijk eerst een elektrochemische op dit scherm zien te krijgen.
Wanneer een elektrochemische cel stroom levert, hebben we deze situatie.
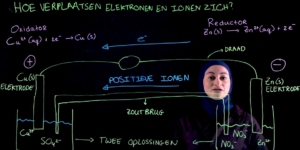
De reductor reageert aan de negatieve elektrode en de oxidator reageert aan de positieve elektrode.
In dit geval zijn dit de volgende half reacties, namelijk de half reactie van de reductor, die elektronen produceert.
En de half reactie van de oxidator, die elektronen opneemt.
Voor de elektrochemische cel betekent dat, dat de stroom van elektronen, dus de beweging van de elektronen, van de reductor gaat, van de min elektrode, naar de oxidator, naar de positieve elektrode.
Dit betekent ook dat de positieve ionen in de zoutoplossingen mee bewegen met die stroom van elektronen, met die beweging.
En die bewegen dus door de zoutbrug dezelfde kant op.
Maar stel nu dat er op een gegeven moment de reactie stopt, omdat bijvoorbeeld een van de reactanten op is, zoals het koper twee plus ion.
Dan kan de elektrochemische cel geen stroom meer leveren.
We kunnen de elektrochemische cel weer opladen door een externe spanningsbron te gebruiken.
Dit is bijvoorbeeld hetzelfde wanneer jij je mobiele telefoon oplaadt, door de oplader erin te steken en hem in het stopcontact te doen.
Voor de elektrochemische cel betekent dat dat we externe energie toevoegen waardoor de half reacties worden omgedraaid.
Ik heb nu de pijlen van de half reacties omgedraaid.
Maar dit betekent natuurlijk dat deze reactie niet meer de oxidator is.
Zowel als dat deze reactie niet meer de reductor is.
Want zoals we weten, een oxidator neemt elektronen op, dus dit is nu de half reactie van de oxidator.
En zoals we weten, in de half reactie van de reductor worden elektronen geproduceerd, dus dit is nu de half reactie van de reductor.
Uit het vorige filmpje hebben we ook onthouden dat de reductor reageert aan de negatieve elektrode en de oxidator reageert aan de positieve elektrode.
Dus ook deze tekens worden hier omgewisseld.
Dit betekent dat nu de zinkelektrode de positieve elektrode is en de koperelektrode de negatieve elektrode.
Zoals we al zeiden, wanneer een elektrochemische cel stroom levert, stromen de elektronen van de negatieve naar de positieve elektrode.
Omdat die hier zijn omgedraaid verandert dus ook de richting van de stroom van de elektronen.
En omdat de positieve ionen in de zoutoplossingen altijd meebewegen met de stroom van die elektronen, gaan ook de positieve ionen de andere kant op, samen mee met de elektronen.
Nou, even samenvatten.
Wanneer een elektrochemische cel wordt opgeladen verandert er heel erg veel.
Ten eerste verandert de richting van de half reacties in de elektrochemische cel.
Dit betekent dat wat eerst de reductor was nu de oxidator is.
En wat eerst de oxidator was nu de reductor is.
Daarmee verandert ook dus de richting van de stroom van de elektronen.
Die bewegen namelijk van de reductor, die elektronen produceert, naar de oxidator, die elektronen opneemt.
Samen met die stroom van die elektronen verandert ook de stroom van de positieve ionen in die zoutoplossing.
Die beweegt namelijk altijd mee met de richting van de elektronen en gaan dus nu ook die kant op.
Uiteindelijk betekent dat ook dat de elektroden van pool wisselen.
Heeft dit je nou geholpen om het beter te begrijpen hoe zo’n elektrochemische cel werkt, kijk dan onze andere filmpjes over elektrochemische cellen op exactwatjezoekt.nl.
Hi, wij zijn Lotte, Noor en Mimi van de Sisters in Science. Wil je meer van ons weten, volg ons dan op Instagram @sistersinscience_NL.