Titaan wordt veelzijdig gevonden onder andere in vliegtuigen en chemische installaties. Het is sterk als staal maar lichter, corrosiebestendig en beter bestand tegen hoge temperaturen. Maar het wordt verreweg het meest toegepast in de vorm van het oxide, bijvoorbeeld in verf en zonnebrandcrème. Het staat in de top tien van meest voorkomende elementen.
Symbool
Ti
Protonen/elektronen
Groep
Isotopen
46Ti, 47Ti, 48Ti, 49Ti, 50Ti
Periode
4
Elektronenconfiguratie
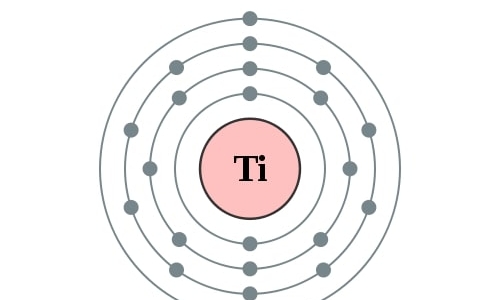
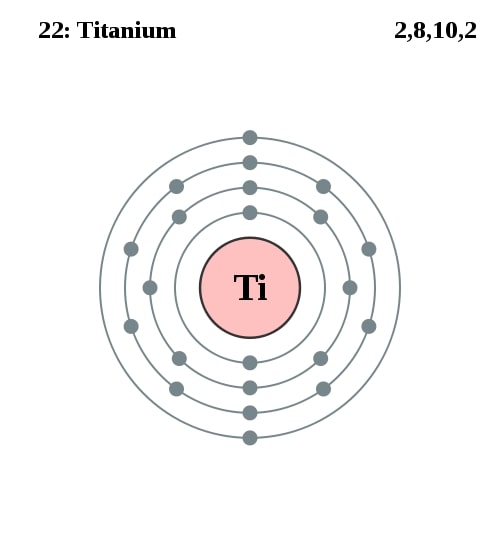
[Ar] 4s2 3d2
Blok
d
Elektronencofiguratie Bohr
2,8,10,2
Bij kamertemperatuur
vast
Elektronegativiteit
1,3 (Pauling)
Dichtheid
4506 kg m-3
Atoomstraal
146 10-12m
Smeltpunt
1668 oC (1941 K)
Relatieve atoommassa
47.9
Kookpunt
3287 oC (3560 K)
Soortelijke warmte
524 J kg-1K-1
Warmtegeleidingscoëfficiënt
21,9 W m-1K-1
Selecteer
Toepassingen
Naam & ontdekking
Voorkomen
Bereiding
Beeld en audio
Toepassingen
Toepassingen
Vliegtuigmotor – ruimtevaart – treinen
Titaan is bijzonder geschikt als constructiemetaal onder veeleisende omstandigheden.
Je vindt het in straalmotoren van vliegtuigen, vanwege de bijzonder grote treksterkte (tot 500 x groter dan die van aluminium), de buitengewoon goede corrosiebestendigheid en de hoge weerstand tegen metaalmoeheid. Bovendien heeft het een zeer hoge hittebestendigheid. Rotorbladen van straalmotoren zijn van zuiver (99,9 %) titaan gemaakt.

Ook in cruciale onderdelen van de dragende structuur (die zeer stevig en toch licht moet zijn) wordt titanium toegepast. Niet alleen in de lucht- en ruimtevaart , maar ook in bijvoorbeeld hogesnelheidstreinen en in duurdere automodellen.
Chemische installaties
Titaan is zeer corrosiebestendig en resistent tegen agressieve stoffen zoals zuren en basen, vanwege een dun, stabiel oxidelaagje. Bovendien beschikt het over een goed warmtegeleidingsvermogen. Vanwege deze eigenschappen wordt het vaak toegepast in leidingen en apparatuur in de chemische industrie.
Bril, horloge, sieraden, piercing
Het lichaam verdraagt titaan zeer goed, het geeft vrijwel geen aanleiding tot metaalallergie. Voor brilmonturen, maar ook voor horloges, piercingmaterialen en sieraden steeds meer gebruik gemaakt van titaan(legeringen). Uiteraard is hier ook van belang dat het metaal sterk en licht is.
Botbreukpen of prothese
In de chirurgie is titaan een veelgebruikt materiaal. Je vindt het onder andere als breukpen (verbindend element tussen bot aan weerszijden van de breuk) en bijbehorende schroeven, maar ook in kunstheupen en andere protheses. Het gaat dan zowel om zuiver titaan, als om titaanlegeringen (bijvoorbeeld met 6 % aluminium en 4 % vanadium).
Pigment: verf, papier
Titaanwit is een veelgebruik pigment vanwege de grote ‘dekkracht’, de grote chemische inertie, de helderheid en de duurzaamheid. Het weerkaatst 96 % van het invallende licht. Titaanwit is niet giftig, in tegenstelling tot loodwit (dat nauwelijks meer gebruikt wordt en vaak verboden is). Titaanwit bestaat uit titaandioxide (TiO2) neergeslagen op een kern van calcium- en bariumsulfaat.

Behalve in verf (voor huisschilders en kunstschilders en in wegenverf) vind je titaanwit in papier, correctielak, email, levensmiddelen (E171), gummi, rubber, glas en kunststof. Het dient hierbij niet alleen als pigment, maar tevens als vulstof.
Het gebruik van titaandioxide is zo groot dat het verantwoordelijk is voor de benutting van ongeveer 95 % van alle titaniumhoudende ertsen. Slechts 5 % van het erts wordt tot titaanmetaal verwerkt.
Geheugenmetaal
Sommige legeringen van titaan en nikkel vertonen bijzonder geheugengedrag. Dit uit zich op verschillende manieren, afhankelijk van de samenstelling. Eén van de effecten is dat een verbogen voorwerp eenvoudig door verwarming weer in de oorspronkelijke toestand is te brengen.
Antennes van kunstmanen worden van titaan-nikkel draad gemaakt en vervolgens opgevouwen tot een bolletje. In de ruimte neemt dit – na verwarmen – weer de oorspronkelijke vorm aan. Geheugenmetaal kent ook medische toepassing, bijvoorbeeld voor beugels (orthodontie) en het herstellen van een verwrongen ruggengraat (scoliose). Een andere toepassing is in (duurdere) BH’s.
Tegengaan luchtverontreiniging
Op een aantal plaatsen zijn proeven gedaan met straatstenen voorzien van titaandioxide. Dit fungeert als katalysator voor de verwijdering van stikstofoxiden (NOx) uit de lucht. Onder invloed van UV straling in het zonlicht worden deze onschadelijk gemaakt. Van grootschalige toepassing is nog geen sprake.
Meer toepassingen
Als element en in legeringen
- Bergsportmaterialen
- Chirurgische instrumenten
- Architectuur: gevelplaten (Guggenheim museum, Bilbao)
- Fietsen (racefietsen en mountainbikes)
- Golfclubs
- Magneten, o.a. voor NMR en deeltjesversnellers (Ti/Nb)
- Maritieme technologie: onderdelen die bestand zijn tegen zeewater
- Veer voor klokken of horloges
In verbindingen
| bleken van textiel en leer | TiCl3,TiCl4 |
| cosmetica (o.a. zonnebrand, tandpasta, lippenstift, poeders) | TiO2 |
| detector Geiger-teller | SrTiO3 |
| TiO2 | |
| etsen van glas | TiCl4 |
| gereedschap, boor- en snijapparatuur (coating) | TiC,TiB2,TiN |
| imitatie-edelsteen (schittert meer dan diamant!) | TiO2, SrTiO3 |
| keramiek | TiC |
| ontspiegelen van lenzen | TiCl4 |
| pigment (geel) | PbTiO3 |
| rookgordijn | TiCl4 |
| slijppoeder | TiC |
Naam & ontdekking
Naam
Titaan is vanwege de sterkte van het metaal genoemd naar de Titanen, het geslacht van krachtige reuzen uit de Griekse mythologie, de kinderen van hemel (Uranus) en aarde (Gaia).
Het Nederlands kent zowel titaan als titanium als benaming voor dit element. Het onderwijs hanteert titaan, maar in het algemeen spraakgebruik lijkt titanium de afgelopen decennia de overhand te hebben gekregen. Mogelijk omdat men in het Engels taalgebied ook over titanium spreekt.
Ontdekking
In 1791 ontdekte de Britse amateurgeoloog William Gregor (foto) titaan in het mineraal ilmeniet, dat hij met behulp van magneten scheidde uit rivierzand. Na verwijderen van ijzer door behandeling met zoutzuur bleef een nieuw oxide (aarde) over, dat alleen oplosbaar was in geconcentreerd zwavelzuur.

Met het door hem ontwikkelde proces om het oxide zuiver in handen te krijgen, legde Gregor de basis voor de productie van titaandioxide via het sulfaatproces (zie tabblad bereiding). In 1795 werd titaandioxide – onafhankelijk van Gregor – door de Duitse chemicus Martin Heinrich Klaproth aangetoond in het mineraal rutiel uit Hongarije.
De uit Nieuw Zeeland afkomstige metallurg Matthew A. Hunter was in 1910 de eerste die zuiver metallisch titaan wist te produceren.
Voorkomen
Voorkomen
Met een aandeel van 0,57 % in de aardkost is titaan verre van zeldzaam. Het staat op plaats negen in de lijst van meest voorkomende elementen.
Ook in meteorieten, op de zon en in andere sterren is titaan aangetoond. Maanstenen bevatten eveneens titaan, tot wel twaalf procent.

Op aarde zijn de belangrijkste titaanhoudende mineralen
- anataas (foto) TiO2
- brookiet TiO2
- ilmeniet Fe+2TiO3
- perovskiet CaTiO3
- rutiel TiO2
- titaniet of sfeen CaTiSiO5
De aanwezigheid van sporen Ti3+ zorgt voor een violette kleur van de betreffende mineralen. In de meeste soorten ijzererts komt ook titaan voor.
Winning
De belangrijkste wingebieden van ilmeniet en rutiel liggen in Brazilië, de Verenigde Staten van Amerika, Canada, Noorwegen, Finland, Portugal, Rusland, Oekraïne, China, Australië, Zuid-Afrika, Maleisië, India, Sierra-Leone, Egypte, Madagaskar en Sri-Lanka.
De mineralen anataas en titaancarbonaat vindt men voornamelijk in Brazilië.
De EU heeft met de Critical Raw Materials Act in 2022 het element titaan op de lijst van schaarse en strategische grondstoffen gezet.
Bereiding
Bereiding
Vroeger
De Zweedse scheikundige Jöns Jacob Berzelius maakte in 1825 zeer onzuiver titaan uit titaandioxide en natrium. De uit Nieuw Zeeland afkomstige metallurg Matthew A. Hunter was in 1910 de eerste die zuiver metallisch titaan wist te produceren. Als hoogleraar bij het Amerikaanse Rensselaer Polytechnic Institute ontwikkelde hij het naar hem vernoemde proces waarin titaantetrachloride (TiCl4) wordt verhit met natrium tot 700-800 °C. Het is weinig efficiënt maar levert wel zeer zuiver titaan (ca. 98,5 %).

Tegenwoordig
Titaan wordt in grote hoeveelheden verkregen via het zogenoemde Kroll-proces. Nadat het erts, bijvoorbeeld ilmeniet, diverse fysische bewerkingen heeft ondergaan, wordt het met behulp van chloor en koolstof omgezet in titaan(IV)chloride:
Het chloride wordt door gefractioneerde destillatie gescheiden en gezuiverd. Reductie met gesmolten magnesium in vacuüm of argon levert vervolgens titaan:
Het titaan is nog verder te zuiveren via omsmelten onder vacuüm.
Bijzonder zuiver titaan is te maken met het in 1925 ontwikkelde proces van de Nederlandse chemici Anton Eduard van Arkel en Jan Hendrik de Boer. Dit betreft thermische ontleding van titaan(IV)jodide in een inerte atmosfeer. Hiervoor wordt onzuiver titaan met wat jood in een vat met zeer lage druk gebracht. Bij ca. 200 °C reageert het titaan tot titaan(IV)jodide. Dit verdampt, waarna het in de nabijheid van een gloeidraad bij zeer hoge temperatuur (ca. 1.300 °C) weer ontleedt in jood en titaan. Het gevormde titaan slaat neer op de gloeidraad.
Titaandioxide
Men bereidt zuiver titaandioxide uit ilmeniet of rutiel via het chloride-proces. De grondstof wordt omgezet in titaan(IV)chloride, dat na zuivering en verbranding zuiver titaandioxide oplevert:

Het voordeel van het sulfaat-proces is dat hiermee ertsen met een geringer titaangehalte zijn te benutten. Het gaat meestal om anataas, dat bij 125 – 200°C wordt behandeld met geconcentreerd zwavelzuur. Dat levert ijzer(II)sulfaat en titaan(IV)sulfaat.
Het ijzersulfaat wordt weggefiltreerd en het titaansulfaat met water omgezet in titaanzuur:
Dit ontleedt vervolgens door verhitting in water en titaandioxide.
Vanwege de problemen met reststoffen in het sulfaatproces schakelt men steeds vaker over op het chloride-proces.