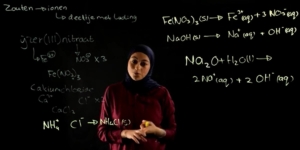Geen zin om een filmpje te bekijken? Hieronder lees je de tekst:
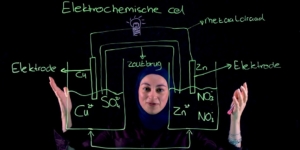
Hoi ik ben Lotte van de Sisters in Science en vandaag ga ik jullie laten zien hoe je met behulp van tabel 48 uit de Binas een volledige redoxreactie kan opstellen en dit heet ook wel de totaalvergelijking.
Vandaag gaan we de totaalvergelijking opstellen, stap voor stap, aan de hand van een oefenopgave uit de oefentoets voor redoxreacties van vwo 5 van exactwatjezoekt.nl.
In deze opgave vragen ze om de totaalvergelijking op te stellen van een mengsel van twee oplossingen.
Nummer 1 is een oplossing van natriumjodide.
En de tweede oplossing is een aangezuurde oplossing van kaliumdichromaat.
Om hiervan de totaalvergelijking op te stellen beginnen we met stap 1, namelijk kijken welke deeltjes er aanwezig zijn.
We hebben hier namelijk twee zouten aanwezig, natriumjodide en kaliumdichromaat.
In molecuulformules is dat NaI en K2Cr2O7.
Maar dit kunnen we natuurlijk niet zo opschrijven in een reactievergelijking, want natriumjodide en kaliumdichromaat zijn aanwezig in oplossing.
En we weten natuurlijk dat in een oplossing deze zouten zich ontleden in de verschillende ionen.
We gaan eerst eens even opschrijven welke ionen er precies allemaal aanwezig zijn.
Bij natriumjodide is dat een natrium Na+ ion en een jodide ion I-.
Bij kaliumdichromaat is dat iets moeilijker.
Is het namelijk het Kalium+ ion K+ en het dichromaat ion, namelijk Cr2O7 2-.
In een oplossing is er natuurlijk ook water aanwezig.
Heel belangrijk is stap 1, is ook kijken of er H+ en OH- deeltjes aanwezig zijn.
In een opgave wordt dit vaak aangegeven door bijvoorbeeld te zeggen of de oplossing in een zuur milieu of een basisch milieu is.
Laten we hier eens kijken of dat het geval is.
We hebben gezien dat onze oplossing kaliumdichromaat aangezuurd is.
Dit betekent dat het een zuur milieu is en dat er dus H+ deeltjes aanwezig zijn.
Dit was dus stap 1 en onthoud altijd goed, kijk altijd naar of een oplossing in een zuur of basisch milieu is.
Voor stap 2 ga ik even in mijn Binas kijken, Binas tabel 48 wat nou de sterkste oxidators en sterkste reductors zijn en daarvan gaan we de halfreacties pakken.
Volgens Binas tabel 48 is het dichromaat onze sterkste oxidator want die staat het hoogst in deze tabel.
En is jodide onze sterkste reductor want die staat het laagst in de tabel.
Hiervan gaan we dus de halfreacties uit de Binas tabel halen en die ga ik nu voor je opschrijven.
Voordat we de totaalvergelijking kunnen opstellen moeten we eerst kijken of deze reactie wel kan verlopen.
Dit doen we door te kijken of de oxidator hoger staat dan de reductor.
Dit bekijken we weer even in Binas tabel 48. Voor deze reactie is dat zo.
Dus check, deze reactie kan verlopen.
Dus stap 3.
Nou, nu kunnen we verder et het opstellen van de totaalvergelijking.
Maargoed hè, in een totaalvergelijking mogen natuurlijk geen elektronen staan, die kunnen we niet zien.
Dus voordat we alle elektronen gaan wegstrepen, moeten we eerst even kijken of de hoeveelheid elektronen die vrijkomt bij de halfreactie van de reductor ook daadwerkelijk wordt opgenomen bij de halfreactie van de oxidator.
We kunnen bij onze reactie zien dat dat niet klopt.
Onze halfreactie van de oxidator, daarbij worden 6 elektronen opgenomen terwijl bij de halfreactie van de reductor er 2 elektronen vrijkomen.
Dit kunnen we makkelijk oplossen door de halfreactie van de reductor te vermenigvuldigen met 3.
En dan komen we op de volgende getallen uit.
Dit was stap 4. Kijken naar of het aantal elektronen in de halfreactie van de oxidator overeenkomt met de elektronen in de halfreactie van de reductor.
En we hebben vermenigvuldigd met 3 dus nu kloppen ze. Stap 4.
Nu kunnen we daar naar stap 5.
Daadwerkelijk onze totaalvergelijking opschrijven.
Dit gaan we doen door alles in één vergelijking te zetten.
En zoals we net hadden gezegd, zien we natuurlijk geen elektronen in onze totaalvergelijking, dus die ga ik gelijk wegstrepen.
Dit was gelijk stap 6. Gelijke deeltjes voor en na de pijl wegstrepen.
Mochten er nou nog andere deeltjes zijn die gelijk zijn voor en na de pijl dan kan je die natuurlijk ook wegstrepen.
In ons geval is dat nu niet zo, dus laten we het staan zoals die nu staat.
Dus onze totaalvergelijking van deze opgave is Cr2O7 2- plus 14H+ plus 6I- wordt 3I2 plus 2Cr 3+ plus 7 H2O.
Tot slot hebben we nog stap 7.
In stap 7 gaan we kijken naar of er coëfficiënten zijn die we kunnen delen door hetzelfde getal.
In onze totaalvergelijking is dat niet zo, dus laten we ‘m staan zoals die hier staat.
Nu hebben we stap voor stap de totaalvergelijking van een mengsel van een oplossing natriumjodide en een aangezuurde oplossing kaliumdichromaat opgeschreven.
Laten we alles nog even samenvatten.
Stap 1: we gaan kijken welke deeltjes er aanwezig zijn.
Hier is het heel belangrijk om te onthouden dat hier ook de deeltjes zoals water H2O en deeltjes zoals H+ en OH- bij horen.
Let daarom goed op in de opgave of je woorden ziet staan zoals aangezuurd of een zuur of basisch milieu.
Stap 2: gaan we in Binas tabel 48 kijken wat de sterkste oxidator en de sterkste reductor is.
Onthoud hierbij goed dat de sterkste oxidatoren bovenaan de tabel staan en de sterkste reductoren onderaan de tabel.
Stap 3: we gaan kijken of deze reactie daadwerkelijk kan verlopen.
Staat de sterkste oxidator boven de sterkste reductor?
Komt er nou uit stap 3 dat we verder kunnen, dan kunnen we de halfreacties gaan opschrijven van de oxidator en van de reductor.
In stap 4 gaan we dan kijken of de hoeveelheden elektronen die worden opgenomen bij de oxidator overeenkomen met de hoeveelheid elektronen die vrijkomen bij de halfreactie van de reductor.
Is dit nou niet zo, zoals bij ons het geval was, kijk dan met welk getal je één van de halfvergelijkingen kan vermenigvuldigen zodat dit wel klopt.
In stap 5 voegen we deze halfreacties samen in de totaalvergelijking.
Waarnaar we in stap 6 de gelijke deeltjes voor en na de pijl kunnen gaan wegstrepen.
In ons geval hebben we de elektronen weggestreept en onthoud altijd goed dat deze niet in de totaalvergelijking komen te staan.
En nu komen we bij de laatste stap, stap 7 en dan kijken we of we de coëfficiënten kunnen delen door een gelijk getal.
Kijk aan, we hebben nu eindelijk onze totaalvergelijking na 7 stappen.
Vond je dit nou interessant en wil je meer weten over redoxreacties? Kijk dan even onze andere filmpjes op exactwatjezoekt.nl.
Wij zijn Noor, Lotte en Mimi van de Sisters in Science.
Wil je meer van ons zien? Volg ons dan op Instagram op SistersinScience_NL.