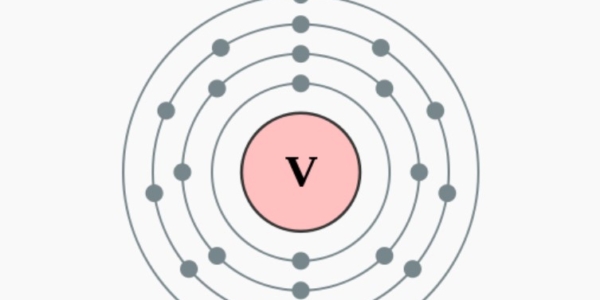
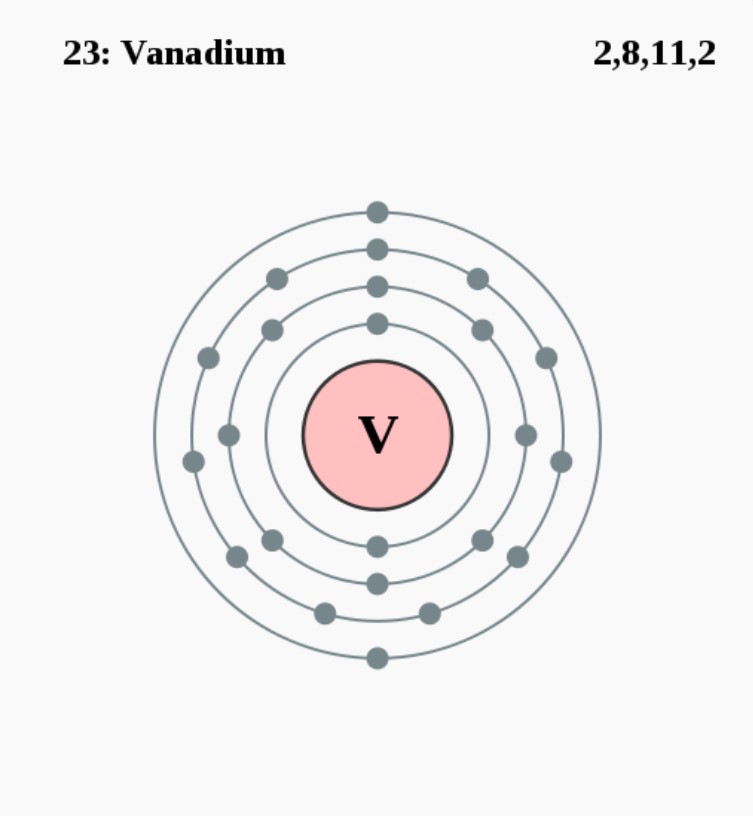
Puur vanadium is een zilvergrijs, zacht en makkelijk te vervormen metaal. Het heeft een goede weerstand tegen corrosie en wordt nauwelijks aangetast door zuren. In zijn zuivere vorm wordt vanadium nauwelijks toegepast. Het is vooral te vinden als legeringselement in staalsoorten, waar het de hardheid en sterkte flink verbetert. Het element is twee keer ontdekt. De eerste vondst in 1801 werd aanvankelijk niet erkend. Na de hernieuwde ontdekking (in 1831) bleek hij toch juist te zijn geweest.
Symbool
V
Protonen/elektronen
Groep
Isotopen
50V, 51V
Periode
4
Elektronenconfiguratie
[Ar] 4s2 3d3
Blok
d
Elektronencofiguratie Bohr
2,8,11,2
Bij kamertemperatuur
vast
Elektronegativiteit
1,5 (Pauling)
Dichtheid
6100 kg m-3
Atoomstraal
131 . 10-12 m
Smeltpunt
1910 oC (2183 K)
Relatieve atoommassa
50.942
Kookpunt
3407 oC (3680 K)
Soortelijke warmte
Warmtegeleidingscoëfficiënt
Selecteer
Toepassingen
Naam & ontdekking
Voorkomen
Bereiding
Beeld en audio
Toepassingen
Toepassingen
Constructiemateriaal/gereedschap/straalmotor
Legeringen van staal met vanadium zijn zeer hard. Je vindt deze in gereedschap, bijlen en messen. Ook voor machineonderdelen die onder zware omstandigheden draaien of bewegen (zoals zuigers, zuigerstangen en krukassen) is vanadiumstaal uitermate geschikt. Andere toepassingen zijn pantserwagens, brandkasten en onderdelen van straal- en raketmotoren.

Veer
Legeringen van ijzer met ongeveer één procent vanadium zijn goed bestand tegen schokken. Ze zijn daardoor zeer geschikt voor de productie van veren.
Aangroeiwerende verf
De snelheid en de brandstofefficiëntie van (zee)schepen nemen af doordat algen en mosselen zich stevig aan de scheepshuid vasthechten. Om dat te voorkomen brengt men onder de waterlijn een aangroeiwerende verf aan. Deze bevat organische vanadium(V)verbindingen als werkzame stof (acetylacetonaten, naftenaten, sulfonaten en octoaten).
Warmteregulerend glas
Een transparante coating van vanadiumdioxide op glas houdt bij hoge temperaturen de infrarode (warmte)straling tegen, zodat het niet te warm wordt. Bij minder hoge temperaturen (onder 29 graden Celsius) verandert de structuur van het vanadiumdioxide en wordt het infrarood wél doorgelaten.

Katalysator zwavelzuurbereiding
De bereiding van zwavelzuur (H2SO4) uit zwavel vindt plaats met vanadiumpentaoxide als katalysator. Het is een zeer efficiënt proces (99,6% rendement) met een lage uitstoot van zwaveldioxide.
Meer toepassingen
Als element en in legeringen
- Constructiemateriaal voor de lucht- en ruimtevaart (Ti,V en TiAl6V4)
- Constructiestaal voor de bouw (0,2 – 1 % V)
- (Kern)reactoren (Ti,V)
- Magneetstaal (Vicalloy: Fe 38 %, V 10 %, Co 52 %)
- Omhulsel van splijtstofstaven voor kernreactoren (Ti,V)
In verbindingen
| Cytostaticum (geneesmiddel, remt de deling van Tumorcellen) vanadoceendichloride, bis(cyclopentadinyl)vanadiumdichloride | (C5H5)2VCl2 |
| Glaskleuring (geel-groen) | V2O5 |
| Katalysator bij het polymeriseren van etheen (plastic) | V2O3 |
| Katalysator bij het verwijderen van NOx uit rookgassen | V2O5 |
| Keramiek, tegels | VSi2 |
| Keramische producten | V2O5, V6O13 |
Naam & ontdekking
Naam
De naam vanadium is afgeleid van ‘Vanadis’, de Scandinavische godin van schoonheid en liefde (beter bekend is onder de naam Freya). Ontdekker Nils Gabriel Sefström (foto) haalde de inspiratie voor die naam uit de grote verscheidenheid aan prachtige kleuren van vanadiumverbindingen.

Ontdekking
Vanadium werd eigenlijk twee keer ontdekt. De Spaans-Mexiaanse mineraloog Andrés Manuel del Río vond het element al in 1801 in Mexicaans looderts. Hij trok zijn claim in toen uit contra-expertise door de Franse chemicus Hippolyte Victor Collet-Descotils zou blijken dat hij slechts basisch loodchromaat had geïsoleerd.
Dertig jaar later, in 1831, trof de Zweedse chemicus Nils Gabriel Sefström (opnieuw) vanadiumverbindingen aan bij zijn studie van ijzererts uit de Falun-mijnen in Midden-Zweden. Later dat jaar bevestigde de Duitser Friedrich Wöhler de ontdekking van Del Río. Sefström stelde de naam vanadium voor en het Mexicaanse erts heet sindsdien vanadiniet.
Ook de productie van metallisch vanadium verliep in twee fasen. Direct na de ontdekking van Sefström claimde zijn landgenoot Jöns Jacob Berzelius dat hij elementair vanadium had geïsoleerd. De Engelse chemicus Henry Enfield Roscoe toonde echter in 1867 aan dat Berzelius vanadiumnitride had gemaakt. Roscoe wist wel zuiver vanadium te maken via de reductie van vanadium(II)chloride met waterstof.
Voorkomen
Voorkomen
Vanadium is een redelijk veel voorkomend element. Met een gewichtsaandeel van 0,012 % in de aardkorst staat het op plaats 20 in de lijst van meest voorkomende elementen.

De belangrijkste vanadiumhoudende mineralen zijn:
| Carnotiet | K2(UO2)2(V2O8).3H2O |
| Descloïziet of mottramiet | PbZn(VO4)(OH) |
| Hewetiet | CaV+56O16.9H2O |
| Montroseïet | (V+3,Fe+3)O(OH) |
| Navajoïet | (V+5,Fe+3)10O24.12H2O |
| Patroniet | VS4 |
| Roscoeliet | K2(V+3,Al,Mg)2(AlSi3)O10(OH)2 |
| Vanadiniet (foto) | Pb5(VO4)3Cl |
| Volbortiet of usbekiet | Cu3(VO4)2.3H2O |
Vanadium is ook aanwezig in diverse ertsen, waaronder ijzererts en titaanerts. Het komt ook voor in aardolie uit Venezuela. Centrales die daarmee worden gestookt produceren vliegas met relatief veel vanadium(V)oxide. Hier wordt weer vanadium uit gewonnen.
Winning
De belangrijkste wingebieden van vanadiumhoudende ertsen liggen in Zuid-Afrika, Rusland, de Verenigde Staten van Amerika, China, Australië en Finland. De EU heeft met de Critical Raw Materials Act in 2022 het element vanadium op de lijst van schaarse en strategische grondstoffen gezet.
Bereiding
Vroeger
De Engelse chemicus Henry Enfield Roscoe was 1867 de eerste die zuiver vanadium wist te maken, via de reductie van vanadium(II)chloride met waterstof.
Tegenwoordig
Tegenwoordig wordt vanadium bereid door reductie van vanadium(V)oxide met calcium, onder hoge druk. Het wordt gewonnen uit vliegas uit aardoliebranders en uit reststromen bij de verwerking van ijzer- en titaanerts en bij de uraniumwinning uit carnotiet.
De vanadiumhoudende grondstof wordt gesmolten met natriumcarbonaat of natriumwaterstofsulfiet, waarbij natriumvanadaat (NaVO3) ontstaat. Na aanzuren, affiltreren van het gevormde polyvanadaat en verhitten, ontstaat vanadiumpentaoxide (V2O5). Het pentaoxide is de uitgangsstof voor de meeste toepassingen van vanadium, zoals bijvoorbeeld het legeren van ijzer (vanadiumstaal).

Om zuiver vanadium te verkrijgen, wordt dit oxide gereduceerd met calcium. Het is ook om te zetten in vanadium(V)chloride of andere vanadium zouten, waaruit vanadium wordt verkregen door reductie met magnesium, of door elektrolyse,.
Kleinere hoeveelheden zeer zuiver vanadium zijn te maken met het in 1925 ontwikkelde proces van de Nederlandse chemici Anton Eduard van Arkel en Jan Hendrik de Boer. Dit betreft thermische ontleding van vanadium(III)jodide in een inerte atmosfeer. Hiervoor wordt onzuiver vanadium met wat jood in een vat met zeer lage druk gebracht. Bij ca. 200 °C reageert het tot vanadium(III)jodide. Dit verdampt, waarna het in de nabijheid van een gloeidraad bij zeer hoge temperatuur (ca. 1.300 °C) weer ontleedt in jood en vanadium. Het gevormde vanadium slaat neer op de gloeidraad.