Deze oefentoets bestaat uit zes vragen over het onderwerp molariteit.
De uitwerking vind je na het openen van alle hints. Let op, als er geen ‘Controleer antwoord’ knop staat, moet je zelf je antwoord controleren met behulp van de hints en uitwerking.
Vraag 1
Sjakie lost 10 gram glucose op in 400 mL water.
Natriumsfosfaat lost op de volgende manier op in water:
Na3PO4 (s) 🡪 3 Na+(aq) + PO43- (aq)
Vraag 2
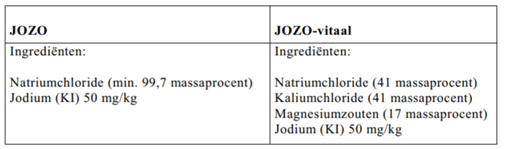
Tamar onderzoekt een potje dat “Jozo-vitaal” bevat.
Ze gebruikt het “Jozo-vitaal” om 100 mL te maken van een oplossing die 0,50 mol natriumchloride per liter bevat.
Vraag 3
Er zijn verschillende oplossingen bekend die azijnzuur (ethaanzuur, CH3COOH) bevatten. Hieronder worden vier soorten genoemd.
- Azijn is een oplossing die 4,0 gram azijnzuur per 100 mL bevat. Het is als een kleurloze maar ook als een bruine vloeistof te koop. In het laatste geval is karamel toegevoegd. Is het azijnzuur verkregen uit alcohol (de zogenoemde natuurlijke methode) dan gebruikt men wel de aanduiding “natuurazijn”.
- Dubbele azijn bevat ten minste 8,0 gram azijnzuur per 100 mL. Het wordt onder andere gebruikt als schoonmaakazijn.
- Kruidenazijn is een azijn waaraan een natuurlijk extract van één of meer kruiden is toegevoegd. In plaats van het extract kunnen ook blaadjes en/of takjes van het kruid worden toegevoegd.
- Azijnessence is een vloeistof die 80 gram azijnzuur per 100 mL bevat.
Uitgaande van azijnessence kan door het toevoegen van water dubbele azijn worden verkregen.
Vraag 4
De productie van anatto in Peru wordt als volgt uitgevoerd:
- 200 kg anattozaden wordt in een vat (vat I) met 400 L 0,014 molair natronloog gedaan.
- De inhoud wordt tien minuten krachtig geroerd.
- De vloeistof wordt in een tweede vat (vat II) overgebracht, de zaden blijven achter in vat I.
- In vat I wordt vervolgens 300 L 0,0063 molair natronloog gedaan.
- Nogmaals wordt gedurende tien minuten krachtig geroerd.
- De vloeistof uit vat I wordt toegevoegd aan de vloeistof in vat II.
- De zaden worden twee keer gewassen met telkens 200 L water.
- Ook deze vloeistoffen worden in vat II gedaan.
- Aan de inhoud van vat II wordt 3,0 L 1,9 molair zwavelzuuroplossing toegevoegd.
- Na enkele uren bezinken wordt de vloeistof afgetapt en de anatto van de bodem geschept.
De zwavelzuuroplossing wordt toegevoegd aan de verzamelde hoeveelheden natronloog.
Hierbij treedt de volgende reactie op: H+ (aq) + OH– (aq) → H2O (l)
Vraag 5
In hard water komen calciumionen en/of magnesiumionen voor. 1,0 DH komt overeen met 7,1 mg Ca2+ per liter.
De hardheid van water wordt bepaald door het aantal mol Ca2+ en/of het aantal mol Mg2+ per liter. Water van 1,0 DH met uitsluitend calciumionen erin (dus geen magnesiumionen) bevat evenveel mol Ca2+ als het aantal mol Mg2+ in water van 1,0 DH met uitsluitend magnesiumionen (dus geen calciumionen) erin.
Vraag 6
Bram onderzoekt de concentratie citroenzuur in een frisdrank. Hij brengt 25,0 mL van deze drank in een erlenmeyer en verwarmt de inhoud enige tijd om alle opgeloste koolstofdioxide te verwijderen. Na afkoelen van de vloeistof moet hij 23,3 mL 0,0500 M natronloog toevoegen om alle citroenzuur te laten reageren.