Deze oefentoets bestaat uit acht vragen over het onderwerp bindingen.
De uitwerking vind je na het openen van alle hints. Let op, sommige vragen hebben geen ‘Controleer antwoord’ knop. Controleer hier zelf je antwoord met behulp van de hints en uitwerking.
Vraag 1
Leg uit welke bindingen aanwezig zijn in de volgende stoffen. De onderstaande hints zijn voor vraag a t/m d.
Je kunt je antwoorden checken met de ‘Controleer antwoord’ knop. In het invulveld vul je alleen de naam van de bindingen in.
Let op: op een toets verwacht een docent de hele uitleg zoals in de uitwerking staat.
Vraag 2
Vraag 3
Vraag 4
Vraag 5
Boorcarbide (B4C) is één van de hardste stoffen die bestaan. Ook heeft de stof een uitzonderlijk hoog smeltpunt van 3036 K.
De extreme hardheid en het hoge smeltpunt van boorcarbide hebben de interesse gewekt van Michiel en Huib. Zij gaan op zoek naar informatie over de microstructuur van boorcarbide.
Michiel vindt in diverse bronnen de volgende structuurformule:
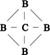
Huib vindt de volgende beschrijving:
Boorcarbide is een keramisch materiaal waarin de atomen elkaar in een driedimensionaal netwerk bijeenhouden met covalente bindingen.
Zij discussiëren over de verklaring van de macroscopische eigenschappen (grote hardheid en hoog smeltpunt) van boorcarbide aan de hand van de informatie die zij hebben gevonden. Samen komen zij tot de conclusie dat deze verklaring niet gegeven kan worden met Michiels informatie, maar wel met Huibs informatie.
Vraag 6
Dit is de structuurformule van hydrochinon.
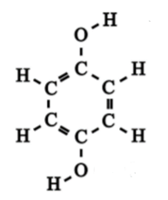
Vraag 7
Jood (I2) is slecht oplosbaar in water. Als er kaliumjodide aan water wordt toegevoegd zijn er jodide (I-) ionen aanwezig. Uit joodmoleculen en jodide-ionen worden I3– ionen gevormd. De I3– ionen worden door watermoleculen gehydrateerd. Hierdoor lost het jood beter op. Een I3– ion wordt schematisch zo weergegeven:
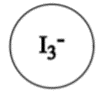
Vraag 8
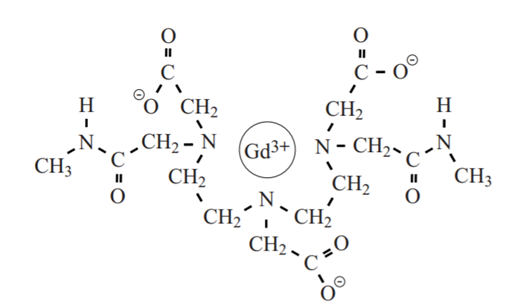
Gadodiamide (zie tekening hierboven) is goed oplosbaar in water. De gadodiamide-deeltjes blijven in de oplossing intact en vallen niet uiteen tot ionen.