kennisclip Alle uitlegfilmpjes
Uitlegfilmpje
Waar zitten de positieve en negatieve elektrode in een elektrochemische cel?
Geen zin om een filmpje te bekijken? Hieronder lees je de tekst:
Hoi, ik ben Lotte van de Sisters in Science en vandaag ga ik jullie laten zien waar in een elektrochemische cel de positieve en de negatieve van de elektrode zitten.
Dit is eigenlijk een standaardvraag die in je examen kan voorkomen.
Neem bijvoorbeeld opgave negentien uit het scheikunde vwo-examen van 2023, tijdvak 1.
De opgave luidt, leg uit of de lithiumelektrode de positieve of de negatieve elektrode is.
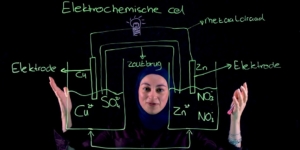
Om deze vraag te beantwoorden gaan we eerst kijken naar de elektrochemische cel die we al eerder hebben getekend in het filmpje ‘Hoe ziet een elektrochemische cel eruit?’.
Ik ga nu deze elektrochemische cel weer tekenen.
In dit voorbeeld gaan we uitzoeken welke van de twee elektrodes nou de positieve en de negatieve elektrode is.
Nou, om dit te kunnen doen gaan we uitzoeken welke half reacties er in deze elektrochemische cel plaatsvinden.
Wil je nou weten hoe je half reacties en een totaal reactie in een redoxvergelijking opstelt, kijk dan ons filmpje ‘Totaalvergelijking opstellen’.
Ik heb alvast opgezocht welke half reacties er in deze elektrochemische cel plaatsvinden en wat de sterkste oxidator is en wat de sterkste reductor is.
Onthoud hierbij goed, de oxidator is hetgeen wat de elektronen opneemt en de reductor is hetgeen wat de elektronen afstaat.
In deze elektrochemische cel is koper twee plus de sterkste oxidator en zink de sterkste reductor.
Ik ga nu de half reacties voor jullie opschrijven.
Ik heb hier de half reacties van deze elektrochemische cel opgeschreven.
Dus onze sterkste oxidator is koper twee plus en onze sterkste reductor is zink.
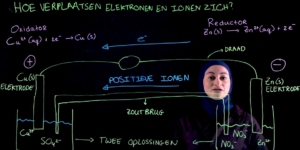
Wat nu heel belangrijk is om goed te onthouden, is dat de oxidator, dus koper, reageert aan de positieve elektrode en onze sterkste reductor, dus zink, reageert aan de negatieve elektrode.
Dit betekent dat in deze elektrochemische cel de koperelektrode onze positieve elektrode is.
En dit betekent dat de zinkelektrode onze negatieve elektrode is.
Dus even samenvatten, hoe pak je zo’n vraag nou aan?
Eerst zoek je uit wat zijn de half reacties in de elektrochemische cel.
Dan ga je kijken wat is nou de sterkste oxidator en wat is de sterkste reductor.
Als laatst moet je goed onthouden dat de oxidator reageert aan de positieve elektrode en dat de reductor reageert aan de negatieve elektrode.
Dus, laten we weer even die examenvraag erbij pakken, opgave negentien uit het scheikunde vwo-examen 2023, tijdvak 1.
Wanneer we door de tekst gaan van deze opgave kunnen we de volgende half reactie lezen.
We zien in deze half reactie, die ik hier mooi in het vakje heb getekend, dat lithium elektronen afstaat.
Nou, dit betekent dat het de reductor is en we hebben net goed onthouden dat de reductor aan de negatieve elektrode reageert, dus daar heb je het antwoord op je vraag.
De lithium elektrode in deze vraag is de negatieve elektrode.
Wil je nou meer weten of die elektrochemische cel? Wil je bijvoorbeeld weten hoe de deeltjes reageren of uit wat voor componenten zo’n elektrochemische cel bestaat. Kijk dan onze andere filmpjes over elektrochemische cellen op exactwatjezoekt.nl.
Hi, wij zijn Lotte, Noor en Mimi van de Sisters in Science. Wil je meer van ons weten, volg ons dan op Instagram @sistersinscience_NL.