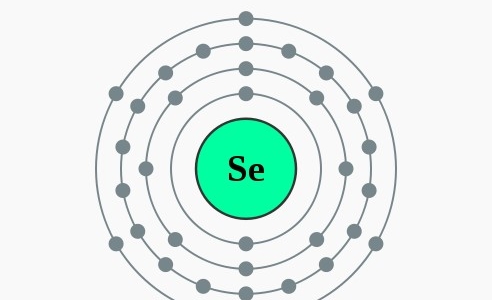
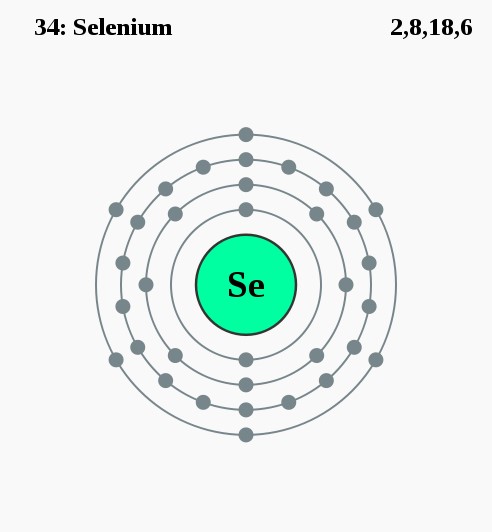
Seleen lijkt op zwavel. Het scheelt maar één letter (in het symbool) en één plaats in dezelfde groep van het periodiek systeem. Chemisch gezien lijken beide elementen erg op elkaar. Seleen is geen metaal maar heeft wel een metallisch uiterlijk. Het komt ook voor als dieprode kristallen of rood poeder. Het is een sporenelement, onmisbaar voor ons biologisch functioneren. Maar in te hoge doseringen kan het toxisch zijn. Veel seleenverbindingen zijn giftig, met name het gasvormige waterstofselenide. Gelukkig stinkt dat enorm, al in zeer lage concentraties.
Symbool
Se
Protonen/elektronen
Groep
Isotopen
74Se, 76Se, 77Se, 78Se, 80Se
Periode
4
Elektronenconfiguratie
[Ar] 4s2 3d10 4p4
Blok
p
Elektronencofiguratie Bohr
2,8,18,6
Bij kamertemperatuur
vast
Elektronegativiteit
2,5 (Pauling)
Dichtheid
4790 kg m-3
Atoomstraal
117 . 10-12 m
Smeltpunt
221 oC (494 K)
Relatieve atoommassa
78.971
Kookpunt
685 oC (958 K)
Soortelijke warmte
350 J kg-1K-1
Warmtegeleidingscoëfficiënt
2.04 W m-1K-1
Selecteer
Toepassingen
Naam & ontdekking
Voorkomen
Bereiding
Beeld en audio
Toepassingen
Toepassingen
Belichtingsmeter
Het elektrische geleidingsvermogen van seleen is sterk afhankelijk van de hoeveelheid licht die er op valt. In het volle daglicht is het geleidingsvermogen ongeveer duizend keer groter dan in het donker. Hiervan maakt men gebruik in belichtingsmeters. Het geleidingsvermogen is dan een maat voor de lichtsterkte van het opvallende licht.

Infrarood optiek
Zinkselenide is een geschikt venstermateriaal voor infrarood licht. Je vindt het onder andere in apparatuur voor infraroodspectroscopie en in de lenzen van koolstofdioxidelasers en nachtzichtkijkers. Het materiaal is in een breed deel van het infrarode spectrum volledig transparant.
Glaskleuring
Rood glas is te maken door de dubbel verbinding cadmiumsulfoselenide (CdS.CdSe) toe te voegen. De hoeveelheid cadmiumselenide in deze pigmentstof bepaalt de kleur. Met 90% CdSe ontstaat een dieprode tot violette kleur, met 60% een roze tot rode kleur en met 30% een oranje kleur. In zeer geringe hoeveelheden (ongeveer tien tot vijftien gram per ton) zorgt het pigment juist voor kleurloos gas aangezien het dan de groene kleur neutraliseert die het gevolg is van de aanwezige ijzerverbindingen. Het pigment geeft ook een rode kleur aan plexiglas en polycarbonaatglas, bijvoorbeeld in auto achterlichten en verkeerslichten.

Anti-roosshampoo
In medicinale anti-roosshampoo wordt een suspensie met ca. 2,4 % seleensulfide (SeS2) toegepast. Seleensulfide gaat ook haaruitval tegen. Seleenverbindingen laten het haar glanzen en maken het voller.
Zonnecel
Seleen is te vinden in zonnecellen, in combinatie met andere elementen, bijvoorbeeld indiumselenide (InSe2) en koper-indium-diselenide (CuInSe2). Koper-indium-galliumselenide (CuInGaSe) is een veelgebruikt materiaal voor dunne, flexibele zonnecellen. Het heeft in die toepassing een bijzonder hoge efficiëntie (zo’n twintig procent).
Geneeskunde
Seleen is een sporenelement, het is onmisbaar voor ons biologisch functioneren. Maar in te hoge doseringen kan het toxisch zijn. Veel seleniumverbindingen zijn giftig, met name het gasvormige waterstofselenide (H2Se). Gelukkig stinkt dat enorm, al in zeer lage concentraties.

Seleen komt onder andere voor in lever, milt, schildklier en hersenen. Seleno-eiwitten kunnen virale mutaties remmen en op die manier groei van kanker tegengaan. Het mechanisme van dit proces is in onderzoek. Selenium lijkt een rol te spelen bij het voorkomen van prostaatkanker. Mannen met een hoger seleniumgehalte in het lichaam hebben tot 30% minder kans deze ziekte te krijgen.
Artritispatiënten hebben een te laag Se-gehalte. (Organische) seleenverbindingen hebben een beschermende invloed op de gewrichten. Seleen heeft een verlichtende werking op pijnlijke gewrichten, activeert de ellen en gaat ontstekingen tegen.
Meer toepassingen
Als element en in legeringen
- Foto-elektrische cel in alarmapparaat, fototelegrafie, radar, geluidsfilmapparaat (grijs Se)
- Gaszuivering
- Halfgeleider in gelijkrichter (diode) o.m. voor oplaadbare batterij (grijs Se)
- Katalysator voor de vetharding
- Materiaalonderzoek (gammastralen van 75Se)
- Metallurgie (verbeteren van de verwerkingseigenschappen)
- Roestvrij staal, chroomstaal, automaten staal
In verbindingen
| Diode | Div. seleniden | |||
| Geneeskunde: | ||||
| – Controle op de aanmaak van bloedplaatjes | 75 Se-verbindingen | |||
| – Behandeling bepaalde bindvliesontsteking (oog) | SeS2 | |||
| – Tegen Se-gebrek | Se-gist | |||
| Katalysator voor het vulkaniseren van rubber | CdSe, Se-diethyldithiocarbamaat, Se(S2CN(C2H5O)2)4 | |||
| Kunstmest (toevoeging) | Div. Se-verbindingen | |||
| Pigment in plastic, verf, inkt, email | CdSe, CdS | |||
| Smeermiddel (toevoeging) | MoSe2, SeO2 | |||
| Transistor | Div. seleniden |
Naam & ontdekking
Naam
De naam seleen is afgeleid van het Griekse woord selènè, dat maan betekent. De elementen seleen en telluur zijn in dezelfde periode ontdekt. Telluur was al vernoemd naar de aarde (Latijn: tellus). Vanwege de grote overeenkomst in eigenschappen tussen beide elementen en het feit dat ze steeds samen werden aangetroffen, werd de naam van seleen afgeleid van de maan.
Behalve seleen wordt soms ook de naam selenium gebruikt – dat is tevens de Engelse benaming voor het element.

Ontdekking
De Zweedse chemici Jons Jakob Berzelius (foto) en Johan Gottlieb Gahn ontdekten seleen in 1817 in achtergebleven materiaal bij de zwavelzuur bereiding. Bij de bereiding was zwavel gebruikt verkregen uit (koper)pyriet uit de Falun-mijnen (Zweden). Eerst toonden ze telluur aan in het residu later seleen.
Voorkomen
Voorkomen
Seleen is een sporenelement, het is onmisbaar voor ons biologisch functioneren. Een gemiddeld menselijk lichaam bevat ongeveer 14 milligram seleen.
Seleen staat op plaats 69 op de lijst van meest voorkomende elementen. Het aandeel in de aardkorst bedraagt 5.10-6 % (op basis van gewicht).

Het element is te vinden in zwavelhoudende ertsen van metalen (bijvoorbeeld pyriet, FeS2 – soms slechts 0,001 %) en in zeldzame mineralen als:
| Berzelianiet | Cu2Se | |||
| Clausthaliet (foto) | PbSe | |||
| Crooksiet | Cu2(Tl,Ag)Se7 | |||
| Naumanniet | Ag2Se | |||
| Tiemanniet | HgSe |
Winning
De belangrijkste wingebieden liggen in Japan, Canada, Rusland en de Verenigde Staten van Amerika.
Seleen wordt ook gewonnen uit het anodeslib van de nikkel-, koper- en loodbereiding, uit restanten van de productie van zwavelzuur en uit stof opgevangen in elektrostatische (rook)gasreinigers. De EU heeft met de Critical Raw Materials Act in 2022 het element seleen op de lijst van schaarse en strategische grondstoffen gezet.
Bereiding
Bereiding
Vroeger
Vrij zuiver seleen werd verkregen via verhitting van ammoniumselenaat, gevolgd door sublimatie.

Tegenwoordig
Anodeslib dat ontstaat bij bereiding van koper door elektrolyse bevat 3 – 25 % seleen en 1 – 8 % telluur. Verbranding van het slib in aanwezigheid van soda resulteert in de omzetting van het aanwezige seleen in seleniet en selenaat, bijvoorbeeld
Hierbij wordt tegelijkertijd het aanwezige tellurium omgezet telluriet en telluraat. Door zwavelzuur aan het verkregen mengsel toe te voegen laat men TeO2 neerslaan en blijft het seleniet in oplossing. Na filtratie wordt SO2 doorgeleid, zodat seleen wordt gevormd:
Het verkregen seleen is redelijk zuiver (99,5 – 99,9 %) maar het is verder te zuiveren via vacuümdestillatie of door omzetting in H2Se (bij 650 °C), gevolgd door ontleding bij 1.000 °C.
Een andere manier van seleen is het uitlogen van seleenhoudend materiaal met een kaliumcyanideoplossing, waarna – na affiltreren – zoutzuur wordt toegevoegd.