Deze oefentoets bestaat uit vijf vragen over het onderwerp organische chemie – reacties.
De uitwerking vind je na het openen van alle hints. Let op, als er geen ‘Controleer antwoord’ knop staat, moet je zelf je antwoord controleren met behulp van de hints en uitwerking.
Vraag 1
Dit is de structuurformule van ethylacetaat:
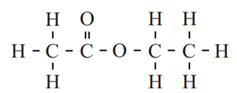
Vraag 2
Ethanol kun je maken door etheen en water met elkaar te laten reageren.
Vraag 3
Hexaan reageert met chloorgas. Hierbij ontstaat C6H11Cl3.
Vraag 4
In een aspergeplant komen asparagusinezuur en de ethylester van asparagusinezuur voor. Van deze stoffen is maar weinig in de plant aanwezig. Toch zorgen ze voor de speciale smaak van asperges. De structuurformule van asparagusinezuur (C4H6O2S2) wordt vaak als volgt schematisch weergegeven:

In deze structuurformule is een aantal van de symbolen C en H weggelaten.
De ethylester van asparagusinezuur is de ester die ontstaat bij de reactie van asparagusinezuur met ethanol.
Asparagusinezuur wordt in het lichaam door enzymen afgebroken. Hierbij ontstaat methaanthiol (CH3SH). Methaanthiol kan vervolgens worden omgezet tot andere zwavelhoudende verbindingen, zoals dimethyldisulfide. Zowel methaanthiol als dimethyldisulfide dragen bij tot de karakteristieke ‘aspergegeur’ van urine. Reeds een half uur na het eten van een portie asperges, waarin ongeveer 1 mg asparagusinezuur zit, kan deze geur worden waargenomen.
Vraag 5
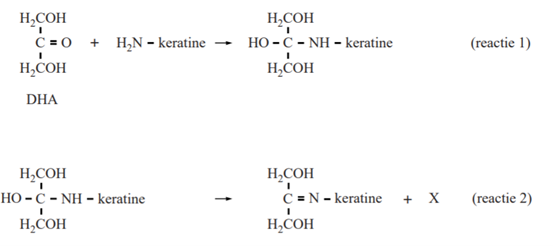
Je kunt een lotion kopen die je op je huid kunt smeren zodat je huid bruin wordt zonder dat je in de zon hoeft te liggen. In deze lotion zit de stof DHA. DHA bindt aan keratine in de huid en daardoor wordt de huid uiteindelijk bruin. Hierbij treden de volgende reacties op: