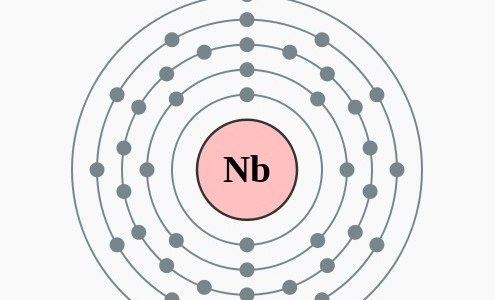
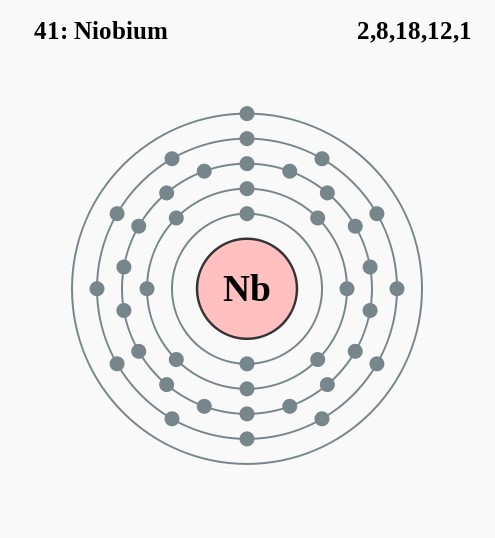
Het zilverachtige, zachte niobium is zeer resistent tegen corrosie. Het komt ongeveer net zoveel voor als lood, maar niet in hoge concentraties. Het is bovendien lastig te winnen vanwege de grote chemische overeenkomsten met tantaal. Het element tantaal staat één positie lager in het periodiek systeem. Niobium is vernoemd naar de Griekse godin Niobe, de dochter van Tantalus. Niobium is te vinden in allerlei High Tech materialen, onder andere in supergeleiders voor MRI scanners en deeltjesversnellers.
Symbool
Nb
Protonen/elektronen
Groep
Isotopen
93Nb
Periode
5
Elektronenconfiguratie
[Kr] 5s2 4d3
Blok
d
Elektronencofiguratie Bohr
2,18,8,12,1
Bij kamertemperatuur
vast
Elektronegativiteit
1,2 (Pauling)
Dichtheid
8570 kg m-3
Atoomstraal
141 . 10-12 m
Smeltpunt
2477 oC (2750 K)
Relatieve atoommassa
92.906
Kookpunt
4744 oC (5017 K)
Soortelijke warmte
265 J kg-1K-1
Warmtegeleidingscoëfficiënt
Selecteer
Toepassingen
Naam & ontdekking
Voorkomen
Bereiding
Beeld en audio
Toepassingen
Toepassingen
Booglaselektrode
Legeringen van niobium met de in het periodiek systeem omringende elementen (zirkonium, molybdeen, vanadium, chroom of wolfraam) zijn zeer hard, corrosiebestendig en bestand tegen zeer hoge temperaturen. Ze worden gebruikt als lasstaaf (elektrode) bij het booglassen.

Pijpleidingen, auto’s
Als toevoeging aan staal bevordert niobium de sterkte en hardheid. Door de vorming van kleine domeinen van niobiumcarbide en niobiumnitrides verbetert het de microstructuur. Het staal is dan beter geschikt voor toepassingen waarbij sprake is van voortdurende belasting (bijvoorbeeld bij zeer hoge temperatuur en extreme kou). Onder andere pijpleidingen zijn gemaakt van niobium gelegeerd staal. Lichte, sterke staalsoorten voor moderne auto’s (HSLA staal: High Strenght, Low Alloy) bevatten eveneens kleine hoeveelheden niobium.
Superlegeringen
Ook in zogenaamde superlegeringen verbetert niobium de mechanische eigenschappen. Zulke legeringen bevatten combinaties van allerlei verschillende metalen zoals bijvoorbeeld nikkel, chroom, kobalt en titanium in wisselende verhoudingen. Deze legeringen zijn ontwikkeld voor gebruik onder zeer veeleisende omstandigheden. Je vindt ze bijvoorbeeld in onderdelen voor straal- en raketmotoren. Een bijzondere superlegering ‘C103’, bestaand uit 89% niobium, 10% hafnium en 1% titanium, werd gebruikt in de hoofdmotor van de Apollo maanlandingsmodules.

Snij gereedschap
Niobiumcarbide NbC is een extreem hard keramisch materiaal, dat onder andere wordt gebruikt om het snijvlak te verstreken van de gereedschappen voor de bewerking (boren, snijden, frezen) van hardmetaal.
Supermagneet
Niobium is een supergeleidend element. Bij de koeling met vloeibaar helium verliest het zijn elektrische weerstand. Dat geldt ook voor legeringen van niobium, bijvoorbeeld met germanium (Nb3Ge), tin (Nb3Sn) en titanium (NbTi). Deze worden gebruik voor de fabricage van supergeleidende draad voor supergeleidende elektromagneten. Dit zijn extreem sterke magneten die onder andere te vinden zijn in MRI scanners (Magnetic Resonance Imaging) en deeltjesversnellers.
Implantaten
Het lichaam verdraagt een legering van niobium en titaan goed. Het vertoont vrijwel geen verschijnselen van metaalallergie of afstoting. Het materiaal is bijzonder sterk en zeer corrosiebestendig. Het wordt daarom gebruikt voor diverse implantaten, bijvoorbeeld een breukpen: een verbindende plaat tussen twee stukken bot.
Meer toepassingen
Als element en in legeringen
- Constructiemateriaal voor o.a. auto’s, hoogspanningsmasten, boorplatforms en bruggen (ferroniobium of niobiumstaal)
- Constructiemateriaal in de lucht- en ruimtevaart (Ti,Nb)
- Gasturbines (Fe,Cu,Ni,Nb)
- Nucleaire industrie: kernreactor, omhulsel van splijtstofstaven (Zr,Nb)
In verbindingen
| Condensatoren | Pb3MgNbO9 |
| Elektrodemateriaal | NbS2 |
| Glas met hoge brekingsindex (voor o.a. optica en brillenglazen) | Nb2O5 |
| Halfgeleiders | NbTi, Nb3Sn |
| Harden van metaal | NbB2 |
| Holografie | LiNbO3 |
Naam & ontdekking
Naam
De naam niobium is afgeleid van Niobe, de dochter van Tantalus (zie ook element 73: tantaal). Deze naam werd gegeven omdat het eerder ontdekte tantaal achteraf uit twee elementen bleek te bestaan. Niobium werd lange tijd columbium genoemd.

Ontdekking
De Engelse chemicus Charles Hatchett ontdekte niobium in 1801 in een mineraal afkomstig uit Massachusetts, dat zich al geruime tijd in het British Museum in Londen bevond. Hij gaf het de naam columbium; het mineraal kreeg de naam colombiet (foto).
Hatchett isoleerde naar alle waarschijnlijkheid een oxide dat behalve niobium ook tantaal bevatte. Net zoals de Zweedse scheikundige en mineraloog Anders Gustaf Ekeberg. Die dacht een jaar later tantaal te ontdekken in een Fins mineraal (tantaliet). Maar ook hij had waarschijnlijk zowel niobium als tantaal in zijn monster.
Jaren van verwarring waren het gevolg. De Engelse chemicus William Hyde Wollaston (foto) probeerde het pleit te beslechten en concludeerde in 1809 dat colombiet en tantaliet hetzelfde oxide opleverden. Hoewel Hatchett een jaar eerder was geweest, stelde Wollaston voor de naam tantaal te handhaven. De ontdekking van Hatchett werd niet erkend en deze trad gefrustreerd terug als hoogleraar.

In 1846 argumenteerde de Duitse chemicus Heinrich Rose dat tantaliet toch twee elementen moest bevatten. Hij stelde voor deze beide te vernoemen naar de kinderen van Tantalys: niobium (naar Niobe) en pelopium (naar Pelops).
Nog eens vijftien jaar later, in de jaren zestig van de negentiende eeuw, kwamen ook andere onderzoekers tot de conclusie dat men met twee elementen van doen had. Maar nog was de controverse de wereld niet uit. De ontdekking van Hatchett werd uiteindelijk erkend, maar hoe moest het element nu heten? Sommigen namen het voorstel van Rose over, anderen (met name de Amerikanen) bleven colombium gebruiken. Pas in 1950 besloot de Internationale Chemieorganisatie IUPAC definitief voor niobium.
Het eerste metallisch niobium werd in 1864 bereid, zowel door de Zweedse chemicus Christian Wilhelm Blomstrand (foto) als zijn Zwitserse collega Jean Charles Galissard de Marignac. Zij reduceerden niobium(V)chloride met waterstof.

Voorkomen
Voorkomen
Het aandeel van niobium in de aardkorst is 2,0.10-3 %. Het staat op plaats 33 in de lijst van meest voorkomende elementen. Het komt ongeveer net zoveel voor als lood (plaats 36), maar nergens in hoge concentraties. Ertsen met slechts één procent niobium zijn al de moeite waard.
De belangrijkste mineralen zijn:
| Betafiet | (Ca,Na,U)2(Ti,Nb,Ta)2 O6.OH |
| Euxeniet (-Y) | (Y,Ca,Ce,U,Th)(Nb,Ti,Ta)2O6 |
| Fergusoniet (-Y) | YNbO4 |
| Ferrocolumbiet | Fe+2Nb2O6 |
| Pyrochloor | (Ca,Na)Nb2O6(OH,F) |
| Tapioliet (foto) | (Fe+2, Mn+2)(Ta,Nb)2O6 |
| Zirkeliet | (Ca,Th,Ce)Zr(Ti,Nb)2O7 |

Ook veel tantaalhoudende mineralen bevatten niobium, bijvoorbeeld stibiotantaliet (SbTaO4) en tantaliet (Fe+2Ta2O6).
Winning
De belangrijkste wingebieden liggen in Brazilië, Canada, Democratische Republiek Congo, Rusland, Australië, Maleisië, Thailand, Oeganda, Nigeria en Noorwegen. Pyrochloor levert 98 % van de grondstof voor de bereiding van niobium. De EU heeft met de Critical Raw Materials Act in 2022 het element niobium op de lijst van schaarse en strategische grondstoffen gezet.
Bereiding
Bereiding
Vroeger
Het allereerste, tamelijk onzuivere niobium werd in 1864 door de Zweedse chemicus Christian Wilhelm Blomstrand bereid. Hij reduceerde niobium(V)chloride met waterstof. In 1906 maakte de Duitse chemicus Werner von Bolton zuiver niobium via reductie van kaliumfluorniobiaat (K2NbOF5) met natrium.

Tegenwoordig
Niobium is vooral een bijproduct van de bereiding van tantaal of tin.
De ertsen worden na een aantal voorbewerkingen gesmolten met natrium- of kaliumhydroxide. Bij verhitten ontstaat dan het pentaoxide van niobium en tantaal. Vervolgens voegt men een mengsel van waterstof- en kaliumfluoride toe, zodat heptafluorotantalaat resp. -niobaat (TaF72- ; NbF72-) ontstaan. Deze tantaal- en niobiumverbindingen worden gescheiden door middel van vloeistofextractie of gefractioneerde kristallisatie. Vervolgens wordt opnieuw het pentaoxide gevormd, dat tenslotte wordt gereduceerd met aluminium of natrium:
In een ander proces behandelt men niobium- en tantaalhoudende materialen met chloor, zodat de chloriden ontstaan. Na scheiding door destillatie worden deze chloriden omgezet in het oxide en volgt reductie met waterstof bij 600 – 650 °C.
Zeer zuiver niobium is te verkrijgen door elektrolyse van complexe niobiumhalogeenverbindingen.