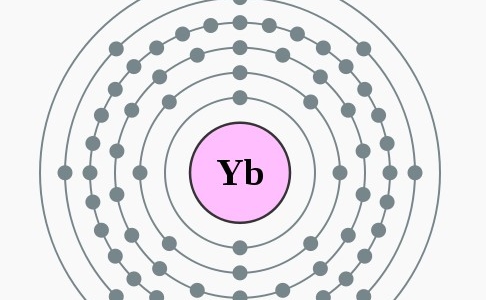
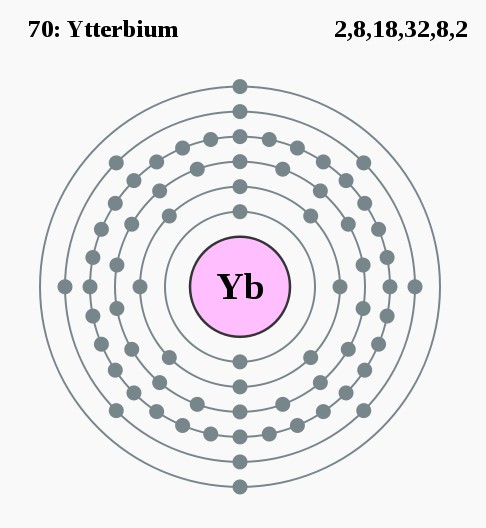
Hett lanthanide ytterbium is vernoemd naar het Zweedse plaatsje Ytterby, net zoals yttrium, erbium en terbium. Ytterby is de vindplaats van de ertsen waarin veel lanthaniden ontdekt zijn. Ytterbium is niet bijzonder zeldzaam maar toch tamelijk lastig te winnen, omdat het minder dan andere lanthaniden de neiging heeft te accumuleren.
Symbool
Yb
Protonen/elektronen
Groep
Isotopen
168Yb, 170Yb, 171Yb, 172Yb, 173Yb, 174Yb, 176Yb
Periode
6
Elektronenconfiguratie
[Xe] 4f146s2
Blok
f
Elektronencofiguratie Bohr
2,8,18,32,8,2
Bij kamertemperatuur
vast
Elektronegativiteit
1,1 (Pauling)
Dichtheid
6900 kg m-3
Atoomstraal
194 . 10-12 m
Smeltpunt
824 oC (1097 K)
Relatieve atoommassa
173,04
Kookpunt
1196 oC (1469 K)
Soortelijke warmte
155 J kg−1 K−1
Warmtegeleidingscoëfficiënt
Selecteer
Toepassingen
Naam & ontdekking
Voorkomen
Bereiding
Beeld en audio
Toepassingen
Toepassingen
Roestvast staal
Ytterbium is een legeringselement in ijzer. Het leidt tot verkleining van de korrels (de microscopische ijzerdomeinen) en verbetert zowel de verwerkingseigenschappen als de sterkte en andere mechanische eigenschappen van roestvast staal.

Laser
Het driewaardige ytterbium ion dient als dopant in moderne lasers, vooral vaste stof lasers en de zogenaamde fiberlasers. De golflengte van het laserlicht ligt afhankelijk van de overige laserelementen rond 1060-1120 nm. Ytterbium is in deze toepassing te vergelijken met erbium. Het speelt een vergelijkbare rol in de signaalvorming en -verwerking in glasvezelnetwerken.
Meer toepassingen
In verbindingen
| Activator van fosforescerende stoffen voor infrarood licht | Yb2O3 | |||
| Halfgeleider | Yb-halogeniden | |||
| Supergeleiding | YbBa2Cu3O7 |
Naam & ontdekking
Naam
De naam ytterbium is (evenals yttrium, erbium en terbium) afkomstig van de vindplaats van het mineraal waarin dit element voor het eerst werd aangetoond: Ytterby, bij Stockholm in Zweden. Het mineraal, dat aanvankelijk ytterbiet werd genoemd, werd later herdoopt tot gadoliniet.
Ontdekking
De Zwitserse chemicus Jean Charles Galissard de Marignac (foto) ontdekte het oxide van ytterbium in 1878 in ytteraarde (afkomstig van gadoliniet).
De Fransman Georges Urbain toonde in 1907 echter aan dat het niet om zuiver ytterbiumoxide ging, maar om een combinatie met lutetiumoxide. Het lukte hem als eerste de twee oxiden van elkaar te scheiden. Ook de Oostenrijker Carl Auer von Welsbach en de Amerikaan Charles James slaagden daar omstreeks dezelfde tijd in.

Toelichting: Zeldzame aardmetalen
Ytterbium behoort tot de zeldzame aardmetalen. De groep omvat de elementen scandium (21) en yttrium (39) en de elementen 57 tot en met 71. Die laatste reeks is ook bekend als de lanthaniden (naar het eerste element uit de reeks: lanthaan).
Zeldzaam wil niet zeggen dat de betreffende elementen weinig op aarde voorkomen. Het gaat hier om een groep elementen die allemaal ontdekt zijn via de isolatie van hun oxide. De term ‘zeldzaam’ vindt zijn oorsprong in het feit dat deze oxiden (aarden) bijzonder moeilijk te herkennen en scheiden zijn. Het duurde meer dan een eeuw voordat ze allemaal ontdekt waren. In dezelfde periode werd bijna honderd keer de ontdekking van andere nieuwe elementen geclaimd.
Na verloop van tijd kwam de term ‘zeldzaam’ ook in zwang als aanduiding van de elementen zelf. Ze werden vaak pas vele jaren na hun ontdekking in zuivere vorm geïsoleerd.
De nieuwe oxiden vinden hun oorsprong voor het grootste deel in twee mineralen: gadoliniet en ceriet. Daaruit werden respectievelijk de oxidenmengsels yttria en ceria ontsloten.
Het relatief ‘zware’ mineraal gadoliniet was in 1787 door de Zweedse chemicus Carl Axel Arrhenius ontdekt in een wingebied voor veldspaat bij Ytterby (in de buurt van Stockholm). Het heette eerst ytteriet, vandaar dat het verwerkingsproduct in 1794 yttria werd genoemd. Men beschouwde Yttria aanvankelijk als het oxide van één enkel element; het latere yttrium (Y). Uiteindelijk bleek het een mengsel van zowel yttriumoxide als de oxiden van de zwaardere lanthaniden: gadolinium, terbium, erbium, dysprosium, holmium, thulium, ytterbium en lutetium.
Ceria werd in 1803 voor het eerst bereid uit ceriet, dat in 1751 was gevonden door de Zweedse chemicus/mineraloog Axel Fredrik Cronstedt. Het leverde de oxiden op van lanthaan en de lichtere lanthaniden: cerium, praseodymium, neodymium, samarium, europium.
Tot het einde van de 19e eeuw waren er geen toepassingen voor (verbindingen van) de zeldzame aarden. De Oostenrijkse wetenschapper Carl Auer Freiherr von Welsbach bracht daar verandering in. Hij gebruikte thorium en cesium ter verhoging van de lichtopbrengst van een gasvlam. De gaspitten werden daartoe in een mengsel van thorium– en ceriumnitraat gedompeld. Bij de verbranding ontstaan dan de oxiden. Ceriumoxide katalyseert de verbranding en door de zeer slechte geleidbaarheid van het thoriumoxide werden de deeltjes zeer heet en geven ze een helder licht.
Met de vinding van Von Welsbach kwam zowel het grootschaliger speuren naar de zeldzame aarden als het zoeken naar toepassingen in een stroomversnelling. Inmiddels zijn meer dan 100 mineralen bekend met zeldzame aardmetalen. Deze metalen kennen specialistische toepassingen in allerlei hoogtechnologische (elektronische) apparatuur. China is verreweg de belangrijkste producent van deze elementen.
Voorkomen
Voorkomen
Op de lijst van meest voorkomende elementen staat ytterbium op plaats 45. Het aandeel in de aardkorst bedraagt 3,2.10-4 % op basis van gewicht.
Ytterbium is niet bijzonder zeldzaam, het komt bijvoorbeeld meer voor dan tin, broom, uranium of arseen. Toch is het lastiger te winnen dan andere lanthaniden omdat het minder de neiging heeft tot accumuleren. Het is in kleine hoeveelheden te vinden in de mineralen.

| Gadoliniet-(Ce) | (Ce,La,Nd,Y)2Fe,+2Be2Si2O10 | |||
| Gadoliniet-(Y) | Y,Fe,+2Be2Si2O10 | |||
| Monaziet-(Ce) (foto) | (Ce,La,Nd,Th)PO4 (ca 0,03 % Yb) | |||
| Monaziet-(La) | (La,Ce,Nd)PO4 | |||
| Monaziet-(Nd) | (Nd,La,Ce)PO4 |
Winning
De belangrijkste wingebieden liggen in Australië, China, India, Brazilië, de Verenigde Staten van Amerika, Maleisië, Rusland, Madagaskar, Noorwegen en Zweden.
Bereiding
Bereiding
Vroeger
Zeldzame aarden werden oorspronkelijk gescheiden op grond van de uiterst kleine verschillen in oplosbaarheid van de metaalhydroxiden en -oxiden in loog. Ook bleek het mogelijk te scheiden op basis van de oplosbaarheid van hun zouten, voornamelijk de oxalaten en sulfaten (met name Ln2(SO4)3.Na2SO4.xH2O, met Ln als symbool voor de lanthaniden). De oplosbaarheid neemt licht toe naarmate de atoommassa van het lanthaniden toeneemt.
De verschillen zijn echter zo klein dat voor een redelijke scheiding vele malen herkristalliseren nodig is. Duizend maal is daarbij geen uitzondering. Om bijvoorbeeld een geringe hoeveelheid zuiver thuliumbromaat te verkrijgen werd zelfs tot vijftienduizend keer geherkristalliseerd.

Tegenwoordig
Na 1950 maakten moderne scheidingsmethoden het makkelijker de zouten van de zeldzame aarden in redelijke hoeveelheden te scheiden. Continue vloeistofextractie bijvoorbeeld, waarbij de waterige oplossing van de zouten wordt geëxtraheerd met tri-n-butylfosfaat. Een andere methode is ionenwisseling, die zouten met een hoge zuiverheid oplevert en doorgaans op wat kleinere schaal wordt toegepast
De nieuwe scheidingstechnieken dienden in de eerste plaats voor de productie van goede splijtstof voor kernreactoren. Daarbij is het van belang uraan- en thoriumertsen te ontdoen van alle sterk neutronen remmende elementen, zoals de lanthaniden. Dit stimuleerde vervolgens ook het zoeken naar toepassingen en daarmee kwam ook een bredere zoektocht naar zeldzame aarden op gang.
Winning uit erts
Het mineraal monaziet bevat (naast 5 – 10 % thoriumoxide, ThO2) enkele procenten van de oxiden uit de zogenaamde yttria-groep (zie tabblad Naam&Ontdekking); andere lanthaniden komen in veel mindere mate voor. Bastnaesiet en allaniet bevatten enkele procenten van – voornamelijk – de oxiden van cerium, lanthaan, neodymium en praseodymium.
Om de lanthaniden te verkrijgen behandelt men het erts, bijvoorbeeld monaziet, met geconcentreerd zwavelzuur bij 200 °C. Daarbij ontstaat een oplossing van de sulfaten van lanthaan, thorium en de aanwezige lanthaniden. Na toevoegen van ammonia slaat eerst het thoriumzout neer. Na toevoegen van natriumsulfaat slaan vervolgens de zouten van de lichtere lanthaniden neer. Na scheiding van de diverse zouten volgt zuivering.
De bereiding van de elementen in zuivere vorm verloopt meestal via elektrolyse van gesmolten zouten. Een andere mogelijkheid is de reductie van oxiden met lanthaan of calcium, of van fluoriden en chloriden met calcium, kalium of natrium. Daarbij wordt het zout gesmolten in een tantalen kroes, gevolgd door reductie (in vacuüm of in een argonatmosfeer) met bijvoorbeeld calciumdamp. Ytterbium wordt bereid door reductie van het oxide (Yb2O3) met cerium of lanthaan.