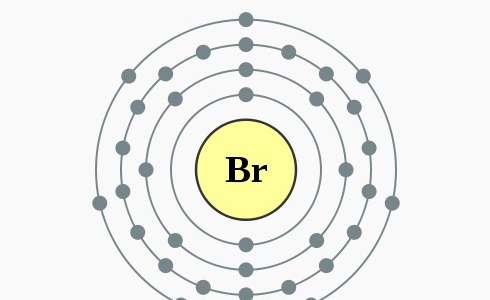
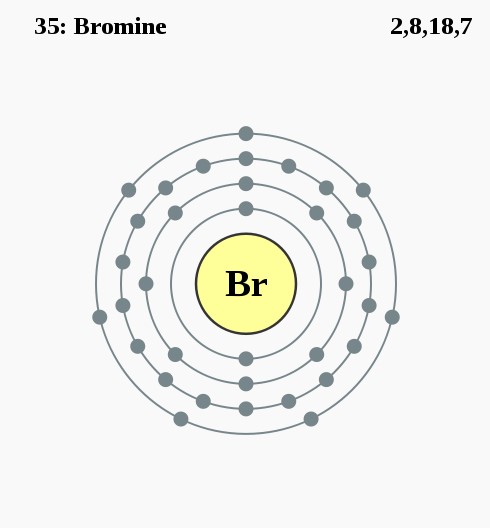
Broom is één van de twee elementen die vloeibaar zijn bij kamertemperatuur en normale druk (de andere is kwik). Elementair broom bestaat als diatomische moleculen, maar komt zodanig op aarde niet in de natuur voor. Broom is een olieachtig halogeen, heeft een dieprode kleur en stinkt behoorlijk. Het is giftig en gevaarlijk bij huidcontact. Broom was het eerste element dat uit zeewater werd gewonnen – vrijwel al het broom op aarde is daarin te vinden.
Symbool
Br
Protonen/elektronen
Groep
Isotopen
79Br, 81Br
Periode
4
Elektronenconfiguratie
[Ar] 4s2 3d10 4p5
Blok
p
Elektronencofiguratie Bohr
2,8,18,7
Bij kamertemperatuur
vloeibaar
Elektronegativiteit
2,7 (Pauling)
Dichtheid
3120 kg m-3 (Br2)
Atoomstraal
114 . 10-12 m
Smeltpunt
-7 oC (266 K)
Relatieve atoommassa
79.904
Kookpunt
59 oC (332 K)
Soortelijke warmte
474 J kg-1K-1
Warmtegeleidingscoëfficiënt
Selecteer
Toepassingen
Naam & ontdekking
Voorkomen
Bereiding
Beeld en audio
Toepassingen
Toepassingen
Haarverzorging
Haar bestaat, net als wol, voornamelijk uit het eiwit keratine. De keratineketens zijn als een spiraal opgerold. Deze structuur wordt onder meer door waterstofbruggen en – veel sterkere – zwavel bruggen bijeengehouden. De kapper die krullen of golven in het haar aanbrengt verbreekt eerst de zwavelbruggen door behandeling met een permanentvloeistof. Als het haar in de gewenste vorm is gebracht moeten de zwavelbruggen weer hersteld worden. Dat gebeurt met een fixeervloeistof, die oxiderende eigenschappen heeft. Kaliumbromaat is een veel toegepaste stof in deze fixeermiddelen (zie ook 16 – Zwavel, haarverzorging)

Vlamvertrager
Broomverbindingen zijn veelgebruikte vlam- of brandvertragende (vlamwerende) middelen, vooral in kunststoffen. Je vindt kunststoffen in behuizingen van allerlei producten (van PC’s tot stofzuigers), in het interieur van auto’s, in speelgoed – eigenlijk bijna overal. Ook synthetische vezels bestaan uit kunststof. Men maakt er kleding, gordijnen, meubelstoffen (ook autobekleding) en nog veel meer van.
Vlamvertragers zijn meestal in hoeveelheden van 2 tot 10% in kunststof aanwezig. Er zijn verschillende soorten, die volgens verschillende mechanismen werken. Als heat-sink beïnvloeden ze de thermische geleidbaarheid van een kunststof, zodat de warmteoverdracht naar het materiaal vermindert en het dus minder snel in brand vliegt. Een ander type ‘verdediging’ is de vorming van een afschermende coating (‘char formation’). Dit bemoeilijk de diffusie van brandbare verbindingen naar het vlamfront. Tenslotte kunnen broomverbindingen die in de vlam terecht komen de (radicaal)reacties aldaar afremmen of stoppen.
Veel gebruikte verbindingen zijn 2,4-dibroomfenol (DBP) en tetrabroombisfenol-A (TBBA).
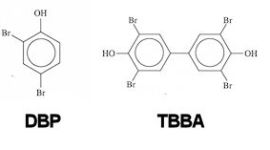
TBBA is een zogenaamde reactieve vlamvertrager die veel in de elektronische industrie wordt gebruikt. Deze wordt ‘ingebakken’ in epoxyharsen voor printplaten.
De niet-reactieve vlamvertrager HBCD (1,2,5,6,9,10-hexabroomcyclododecaan) wordt gemengd met kunststoffen, bijvoorbeeld polystyreen.
Geneesmiddel
Broom is in diverse geneesmiddelen te vinden, bijvoorbeeld:
- Bromazepam, (C14H10BrN3O), een kalmeringsmiddel.
- Broomhexine (2-amino-3,5-dibroom-N-cyclohexyl-N-methylbenzylamine, C14H20Br2N2..HCl), een middel dat het ophoesten van slijm bevordert.
- Broomperidol, (C21H23BrFNO2), een anti-psychotisch middel.
- Broomcryptine, (C32H40BrN5O5), een borstvoedingsremmer bij kleine dosis en een anti-Parkinsonmiddel bij grote dosis.

Fotopapier, film
Fotografisch film- en papiermateriaal bestaat uit een lichtgevoelige laag – meestal zilverbromide – op een drager. Door licht ontleedt het zilverbromide, waarbij zilver ontstaat:
Indicatie van het broomgehalte:
- Film: 3,7 g.m-2
- Fotopapier: 1,5 g.m-2
- Föntgenfilm: 5,2 g.m-2
Meer toepassingen
Als element en in legeringen
- Bleken van textiel(broomwater)
- Baterzuivering
In verbindingen
| Aardoliewinning, oplossingen met hoge soortelijke massa | CaBr2, ZnBr2, NaBr | |||
| Absorptiemiddel voor waterdamp | LiBr | |||
| Batterij | ZnBr | |||
| Bleekmiddel voor wol | KBrO3 | |||
| Blusmiddel, voor computerinstallatie, luchtvaart, auto’s | Broomdifluormethaan, broomtrifluormethaan | |||
| Cosmetica, kleurstof | Broomkresolgroen | |||
| Desinfectiemiddel | 4-broomfenol | |||
| Forensisch onderzoek, aantonen zweetsporen | Broomfenolblauw | |||
| Halogeenlamp | Methylbromide | |||
| Houtbeschermingsmiddel | 2,4,6-tribroomfenol | |||
| Metaalbeits | NH4Br | |||
| Ontwikkelvloeistof in de fotografie | KBr, NH4Br |
Naam & ontdekking
Naam
De naam broom is afgeleid van het Griekse woord bromos voor stank. Aanleiding hiertoe was de onaangename, prikkelende geur van broom.
Ontdekking
De Duitse chemicus Carl Jacob Löwig onderzocht in 1825 moeraswater dat (naar achteraf bleek) rijk was aan magnesiumbromide. Löwig, destijds als 22-jarige in de leer bij Leopold Gmelin in Heidelberg, had bij een van zijn proeven het chloride uit het water verwijderd en leidde vervolgens chloorgas door de verkregen oplossing. Hierbij nam hij het ontstaan van een nieuwe stof waar: broom. Hij isoleerde het nieuwe element door extractie met ether gevolgd door destillatie.

Een jaar later beschreef de Fransman Antoine-Jérôme Balard (foto) juist afgestudeerd aan de Ecole de Pharmacie in Parijs, dezelfde ontdekking. Hij verkreeg broom door het inleiden van chloorgas in een extract van zeewier-as waaruit het chloride was verwijderd. Ook in uit zeewater wist hij broom te isoleren.
Omdat Löwig de eerste was die broom isoleerde, en Balard de eerste die er over publiceerde, delen beide onderzoekers nu de eer van de ontdekking van broom. Löwig schreef overigens in 1829 nog wel een uitgebreide monografie over ‘broom en zijn chemische betrekkingen’.
Voorkomen
Voorkomen
Broom staat op plaats 50 in de lijst van meest voorkomende elementen in de aardkorst. Het aandeel bedraagt 2,4.10-4 % op basis van gewicht. 99 % van alle broom op aarde komt voor in zeeën en oceanen. De oceanen bevatten 68 mg broom per liter en de Dode Zee zelfs 5 g per liter. Het element komt altijd voor in verbindingen.

De belangrijkste broom bevattende mineralen zijn:
- Broomargyriet, AgBr
- Emboliet (foto), Ag(Br,Cl)
Winning
De belangrijkste wingebieden liggen in de Verenigde Staten van Amerika (North Carolina, Arkansas, Michigan) en in Palestijn (Dode Zee). Andere wingebieden liggen in het Verenigd Koninkrijk, Frankrijk, Japan, Italië, Turkmenistan, Oekraïne, Azerbeidzjan en Duitsland.
Bereiding
Bereiding
Vroeger
Broom werd gewonnen uit afvalloog ontstaan bij de winning van natriumchloride uit zoutlagen. Bij een behandeling met bruinsteen en zwavelzuur reageren de bromiden uit het loog volgens
Een andere methode was de elektrolyse van bromide-oplossingen, waarbij aan de positieve elektrode broom wordt gevormd:

Tegenwoordig
Broom wordt meestal bereid via het door leiden van chloor in bromide-rijke waterige oplossingen bij een pH van ongeveer 3,5: